题目内容
【题目】(1)用元素符号或化学式填空.
①硅元素__。
②氮气__。
③2个氢氧根离子__。
④两个二氧化硫分子__。
(2)如图体现了稀盐酸和氢氧化钠溶液反应的实质,请回答有关问题.
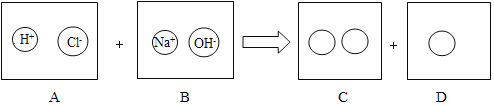
①在如图C、D中的圆圈内填入适当的化学式或离子符号:C中__、__.D中__.
②用化学方程式表示图中所体现的化学反应__.
③以上变化的反应基本类型是__.
【答案】Si N2 2OH﹣ 2SO2 Na+ Cl﹣ H2O HCl+NaOH=NaCl+H2O 复分解反应
【解析】
(1)①硅元素的元素符号为:Si;
②氮气属于气态非金属单质,在元素符号的右下角写上表示分子中所含原子数的数字,其化学式为:N2;
③离子的表示方法:在表示该离子的元素符号右上角,若表示多个该离子,就在其元素符号前加上相应的数字,故2个氢氧根离子可表示为:2OH﹣;
④分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,所以两个二氧化硫分子可表示为2SO2;
(2)①中和反应的实质是氢氧根离子和氢离子反应生成水的过程,氯化钠是钠离子和氯离子构成的,所以C中是Na+、Cl﹣,D中H2O;
②氢氧化钠和盐酸反应生成氯化钠和水,化学方程式为:HCl+NaOH=NaCl+H2O;
③该反应是两种化合物互相交换成分生成另外两种化合物的反应,属于复分解反应.

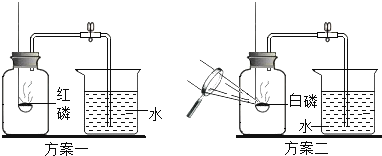
【题目】下图是实验室制备气体的部分装置。
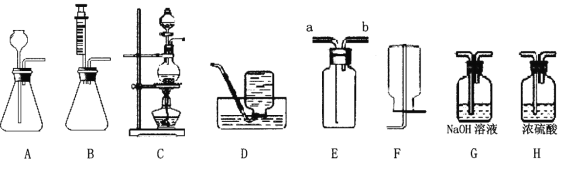
(1)上图装置可以制取不同气体,请完成下表空格。
反应物和反应条件 | 制取的气体 | 发生装置(填字母) | 收集装置(填字母) |
H2O2溶液和MnO2固体,常温 | ______ | A或B | 或E |
亚硫酸钠(Na2SO3)固体和浓硫酸,常温 | SO2 | ______ | E |
甲酸( HCOOH)和浓硫酸,加热 | CO | ______ | D |
(2)用A装置制取O2时,反应的化学方程式为____________________,若要得到干燥的O2,所选择装置的连接顺序为:A→____→ _____ (填字母序号)。
(3)用E装置收集SO2时,气体应由(填“a”或“b”)________端进入。
【题目】实验室存放盐溶液的柜子里,有一瓶无色溶液的标签因受到腐蚀而破损,如图所示。某兴趣小组同学对其成分进行探究。
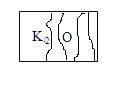
(提出问题)这瓶是什么溶液呢?
(猜想与假设)经了解得知,这瓶无色溶液可能是
碳酸钾、硫酸钾、氯化钾、硝酸钾中的某一种溶液。
(推理分析)小组同学为了确定该溶液的成分,他们进行了以下
(1)甲同学根据物质的组成元素认为一定不可能是________溶液。
(2)乙同学认为也不可能是硝酸钾溶液,他的依据是______________。
(设计实验)为了确定该溶液究竟是剩余两种溶液中的哪一种,丙同学设计了如下实验:
实验操作 | 实验现象 | 实验结论 |
取少量该溶液于试管中,逐滴加入氯化钡溶液 | 产生白色沉淀 | 该溶液一定是碳酸钾溶液 |
(实验反思)
(1)丁同学认为丙的结论不合理,理由是___________________________。
(2)在丙同学实验的基础上,丁同学继续进行实验,实验方案如下:
实验操作 | 实验现象 | 实验结论 |
取丙同学实验所得的白色沉淀于试管中,滴加适量的_________,振荡 | _________,沉淀溶解 | 该溶液是碳酸钾溶液。 反应的化学方程式是_____ |
(3)为防止标签受到腐蚀,倾倒液体时应注意:____________________。