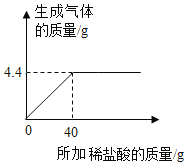
题目内容
【题目】下图是实验室制备气体的部分装置。
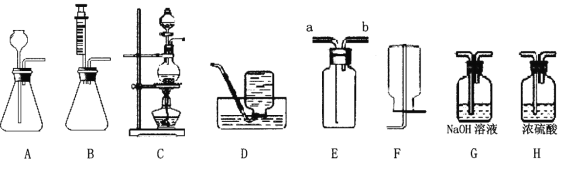
(1)上图装置可以制取不同气体,请完成下表空格。
反应物和反应条件 | 制取的气体 | 发生装置(填字母) | 收集装置(填字母) |
H2O2溶液和MnO2固体,常温 | ______ | A或B | 或E |
亚硫酸钠(Na2SO3)固体和浓硫酸,常温 | SO2 | ______ | E |
甲酸( HCOOH)和浓硫酸,加热 | CO | ______ | D |
(2)用A装置制取O2时,反应的化学方程式为____________________,若要得到干燥的O2,所选择装置的连接顺序为:A→____→ _____ (填字母序号)。
(3)用E装置收集SO2时,气体应由(填“a”或“b”)________端进入。
【答案】O2 A或B C 2H2O2![]() 2H2O+O2↑ H E a
2H2O+O2↑ H E a
【解析】
(1)过氧化氢在二氧化锰作催化剂的条件下反应生成水和氧气,用来在实验室中制取氧气,故填O2;
亚硫酸钠(Na2SO3)固体和浓硫酸在常温反应生成硫酸钠、水和二氧化硫,应选用固液常温发生装置,故填A或B;
甲酸( HCOOH)和浓硫酸在加热条件下反应生成一氧化碳,是液体在加热条件下反应生成气体,应选择液体受热发生装置,故填C。
(2)用A装置制取O2的反应是过氧化氢在二氧化锰作催化剂的条件下反应生成水和氧气,故反应的化学方程式写为:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
要得到干燥的O2,要先将氧气干燥,再选择向上排空气法收集氧气,故填HE。
(3)SO2的密度大于空气的密度,所以用E装置收集SO2时,气体应由长管进入瓶中,故填a。

 天天练口算系列答案
天天练口算系列答案【题目】阅读下面科普短文。
甲醛(CH2O)是很重要的化工材料,通常为无色气体,有特殊的刺激气味,易溶于水。但室内空气中甲醛是影响人类身体健康的主要污染物。表一列举了室内空气的主要污染物及来源。
污染源 | 污染物 |
建筑材料 | NH3、甲醛(CH2O)、苯(C6H6)、甲苯(C7H8)、石棉纤维等 |
家具 | 甲醛(CH2O)、甲苯(C7H8)等 |
办公用品 | O3、电磁辐射等 |
烹饪 | CO、NO2、SO2、PM10等 |
室内微生物 | 结核杆菌、霉菌等 |
表一
国家标准规定:居室空气中甲醛浓度<0.08 mg/m3.有关装修材料甲醛释放量的研究中,相关人员监测了室内空气污染物含量随时间的变化。图一是同一居室在装修后0~3、5~8、9~12、12~18个月后,室内空气中甲醛、苯、氨含量的超标率随时间变化曲线如下:
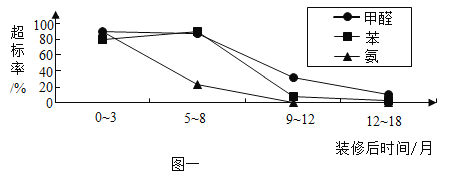
因此,我们需要采取措施尽可能去除室内甲醛,但传闻去除甲醛的方法有很多。
传闻1:用水、醋、红茶泡水来去除甲醛
事实上即使在房间内放一百盆水,其实吸附效果不会比一小包活性炭强多少。实验结果表明,空气中相对湿度增加10%,室内甲醛释放量会增加5%左右。
传闻2:用植物净化去除甲醛
植物能够通过光合作用吸入甲醛,但该方法的效果极为有限。以吸收甲醛效率较高的绿萝为例,每小时吸甲醛20ug(1ug=10-6g)。以一个100m2,房高3m,甲醛值为0.2mg/m3的新装修房间来讲,需要1800盆绿萝,几乎要把整个房子空间添满,才能将甲醛降为0.08 mg/m3。
传闻3:用柚子、菠萝等水果吸附甲醛
在相同密封仓中,放柚子皮的实验仓甲醛含量是空白仓的十倍。因放柚子皮后,实验仓温度增大,甲醛释放量增加。柚子皮、菠萝等不但无法去除甲醛,还会使室内甲醛含量增加,只是水果的味道把甲醛的味道掩盖住了。
通过实验研究,相对有效的去除方法是通风法、吸附法和光触媒法。
通风法是通过室内空气的流通,降低室内甲醛浓度,优点是效果好,但缺点是时间长。吸附法,首选活性炭,不过活性炭吸附材料需要定期更换,以免吸附饱和后再散发出来。近几年,装修市场推出硅藻泥墙面,据研究表明也可以净化空气。硅藻泥的主要成分是硅藻土,是由水生浮游类生物沉积而成。电子显微镜显示,硅藻土粒子表面具有无数微小的孔穴,功能与活性炭相似。正是这种多孔的结构,使硅藻泥成为具有净化空气功能的内墙装饰材料。
“光触媒”是一种纳米级材料,具有极强净化空气功能。图二就是“光触媒”技术应用于去除甲醛、甲苯等有害物质的原理图。
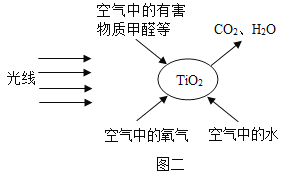
依据文章内容回答下列问题:
(1)依据表一的信息,室内空气中甲醛的污染源是______。
(2)依据文中图一,分析在其它条件相同时,室内甲醛浓度与时间关系是______。
(3)与室内空气中甲醛浓度的大小有关的因素包括______(填序号)。
A 室内温度 B 室内湿度 C 室内空气流通量
(4)请写出光触媒除甲醛法发生反应的化学反应方程式:______。
(5)下列说法正确的是______(填序号)。
A 甲醛的沸点比水低
B 室内闻不到刺激性气味,室内空气中一定不含甲醛
C 硅藻泥通过吸附污染物净化了空气
D 吸收、转化、降低室内污染物的浓度都可以改善室内空气质量
【题目】小昊同学欲通过化学实验验证“质量守恒定律”,进行了下列实验探究。
(实验设计)根据实验目的,小昊确定以“铁和硫酸铜溶液”为研究对象,设计的实验装罝如图二所示。
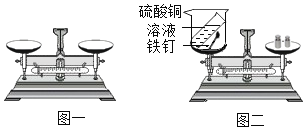
(进行实验)
实验步骤 | 实验现象与记录 | 解释或结论 |
①调零 |
| 如图一所示,调节平衡螺母天平无法平衡的原因是 _________; |
②称量铁钉的质量 | 记录称量数据为5.6g |
|
③称量硫酸铜溶液和烧杯的总质量 | 记录称量数据为113.2g |
|
④铁钉放入盛有硫酸铜溶液的烧杯中 | _____________________________________________ | 该反应的化学方程式为__________________________; |
⑤充分反应后,按如图二方式放好仪器和药品并称量 | 记录称量数据为_____________ | 该反应遵守质量守恒定律 |
(交流反思)(1)下列物质的溶液可以替代硫酸铜溶液直接利用图二装置完成上述实验的是______(填序号)。 A.硫酸铝 B.稀硫酸 C.硝酸银 D.乙醇
(2)实验结束后,过滤步骤⑤烧杯中的混合物,洗涤和干燥后称量固体的质量为5.8g,则该实验中生成铜的质量为___________g。