题目内容
【题目】下列图像分别与选项中的操作项对应,其中不合理的是
A. 往一定量的NaOH溶液中滴加稀盐酸至过量
往一定量的NaOH溶液中滴加稀盐酸至过量
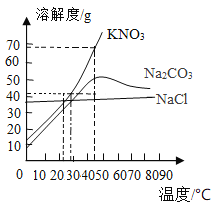
B. 某温度下,将KNO3固体不断地加入水中
某温度下,将KNO3固体不断地加入水中
C.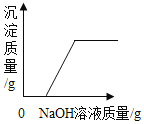 向一定量CuSO4溶液和稀硫酸的混合溶液中滴加NaOH溶液
向一定量CuSO4溶液和稀硫酸的混合溶液中滴加NaOH溶液
D.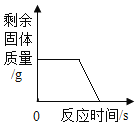 持续不断地加热一定质量的高锰酸钾固体
持续不断地加热一定质量的高锰酸钾固体
【答案】D
【解析】
A、往一定量的NaOH溶液中滴加稀盐酸至过量,一开始,氢氧化钠显碱性,pH>7,氢氧化钠与稀盐酸反应生成氯化钠和水,随着的反应的进行,pH逐渐减小,稀盐酸过量时,pH<7,不符合题意;
B、某温度下,将KNO3固体不断地加入水中,随着硝酸钾固体的不断加入,溶质质量分数逐渐增加,待溶液达到饱和后,溶质质量分数不再变化,不符合题意;
C、向一定量CuSO4溶液和稀硫酸的混合溶液中滴加NaOH溶液,氢氧化钠先与稀硫酸反应生成硫酸钠和水,故一开始无沉淀产生,待稀硫酸完全反应后,氢氧化钠再与硫酸铜反应生成氢氧化铜沉淀和硫酸钠,随着反应的进行,沉淀质量不断增加,待硫酸铜完全反应后,沉淀质量不再变化,不符合题意;
D、持续不断地加热一定质量的高锰酸钾固体,高锰酸钾在加热的条件下分解为锰酸钾、二氧化锰和氧气,有气体生成,剩余固体质量不断减小,待高锰酸钾完全反应后,不再变化,反应后,有锰酸钾和二氧化锰生成,固体质量不会减少至零,符合题意。
故选D。

 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案【题目】金属的用途与性质密切相关。
(1)如图所示赤铁矿的主要成分是________(填名称);

(2)家用电线常用铜制,但在高压远距离输电中,常用铝代替铜,请根据信息分析,其原因是_______________;
铜 | 铝 | |
密度/(gcm-3) | 8.92 | 2.70 |
地壳中含量(质量分数/%) | 0.007 | 7.73 |
导电性(以银的导电性为100做标准) |
| |
(3)在空气中,铝具有很好的抗腐蚀性,其原因是______;
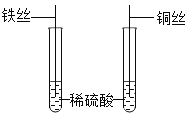
(4)为探究铁、铜的金属活动性,分别将铁丝、铜丝插入稀硫酸中(如图所示),说明铁比铜的金属活动性更强的实验现象是______,反应的化学方程式是______,后来,小贝选择两种药品,通过一步实验,也达到了实验目的,她选用的药品是 ____(写出一种药品组合即可);
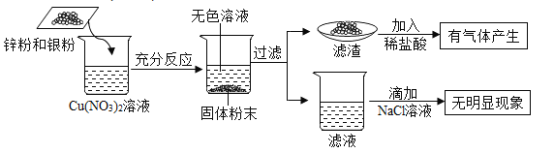
(5)将一定质量的铁粉加入到Al(NO3)3、Cu(NO3)2、AgNO3三种物质的混合溶液中,充分反应后过滤,得到滤液和滤渣。下列有关说法正确的是____(填字母)。
A 若滤液为蓝色,则滤渣中一定有银,可能有铜
B 若滤渣中含有银、铜、铁,则滤液中一定含有Al3+、Fe3+、NO3﹣
C 若滤液为浅绿色,则滤渣中一定含银、铜、铝
D 若滤渣中加稀盐酸无气泡产生,则滤液中一定有Al3+、Fe2+、Cu2+,可能有Ag+
【题目】Na2CO3和NaHCO3有相似的化学性质,都能与酸、某些碱反应。但碳酸钠稳定,而 NaHCO3受热分解:2NaHCO3![]() X+H2O+CO2↑。
X+H2O+CO2↑。
(1)生成物X的化学式为______。
(2)工业上用碳酸钠制烧碱的化学反应方程式为______。
(3)同学们在探究其化学性质实验后,将剩余固体药品集中放在烧杯中。小明为了弄清剩余固体的成份,进行了如下的探究:
(提出猜想)剩余固体是:I.Na2CO3;Ⅱ.NaHCO3;Ⅲ.______。
(进行实验)
操作 | 现象 | 结论 |
①取少量剩余固体于试管中,加入足量水,充分溶解后,滴加几滴酚酞溶液。 | 溶液由无色变红色。 | 剩余固体一定有: ______ 。 |
②取适量剩余固体于试管中,固定在铁架台上,充分加热。 | 白色固体质量减少, 试管内壁有较多水珠出现。 |
(结论分析)
①据上述实验现象,小明认为猜想Ⅲ正确。但有同学认为小明的判断不严谨,因为猜想______也有相同现象。
②同学们讨论后认为,如要确定剩余固体成分,小明只要做实验操作②,并补充操作______,再通过______即可得出结论。
(拓展反思)
有同学提出,碳酸钙和碳酸氢钙能不能互相转化呢?小明认为可以,因课本“资料卡片”中介绍的《石笋和钟乳石的形成》就是“CaCO3→Ca(HCO3)2→CaCO3”的过程。则“CaCO3→Ca(HCO3)2”化学反应方程式为______。