题目内容
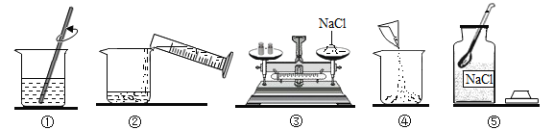
【题目】某化学兴趣小组在实验室里完成了以下实验:称取5.0g粗盐(只含泥沙)进行提纯,并用提纯后获得的精盐(NaC1) 配制溶质质量分数为6%的NaCl溶液50g。实验的操作流程如下图所示,请你根据信息回答下述问题:

(1)步骤一中, 操作X的名称是__________;步骤二中, 实验步骤Y的名称为____________。
(2)粗盐加水溶解过程中用到了玻璃棒不断搅拌,它的作用是____________。
(3)某同学所得精盐比其他同学明显要少,原因可能是____________。
(4)配制50g质量分数为6%的NaCl溶液时,某同学量取水时仰视47mL刻度处,则他所配制的NaCl溶液质质量分数____________(填“大于 ”“小于”或“等于”)6%.
【答案】过滤 称量 加快氯化钠的溶解速率 加水溶解时,水量少了,氯化钠没有完全溶解或蒸发时有部分氯化钠飞溅 小于
【解析】
(1)大于100纳米不溶的固体小颗粒悬浮于液体里形成的混合物叫悬浊液,经过操作X变成了溶液,说明操作X将固体与液体进行了分离,除去了不溶性物质,故操作X的名称是:过滤;
配制一定溶质质量分数的溶液的步骤为:计算、称量、溶解、装瓶,故步骤Y的名称为:称量;
(2)玻璃棒的作用是:搅拌,加快氯化钠的溶解速率,故填:加快氯化钠的溶解速率;
(3)所得精盐偏少,可能是:加水溶解时,水量少了,氯化钠没有完全溶解,或者蒸发时,有部分氯化钠飞溅溅出等;
(4)仰视读数,读取数值小于实际数值,使量取水的质量偏大,溶液质量偏大,溶质质量不变,溶质质量分数偏小,故所配制的NaCl溶液溶质质量分数小于6%。

【题目】某合金的主要成分为 Zn、Fe 和 Cu。研究小组利用该合金制成的机械零件废弃物制取高纯度的 ZnO,其部分工艺流程如下图所示。请回答:
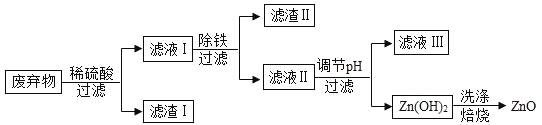
(1)实验前将废弃物处理成粉末的目的是:_________;
(2)滤渣Ⅰ中一定有_________;
(3)加酸溶解废弃物时,需要通风并远离火源,其原因是_________;
(4)焙烧 Zn(OH)2 发生分解反应的化学方程式为_________;
(5)研究小组利用上述的废弃物测定稀盐酸的溶质质量分数,他分四次向 182.5g 稀盐酸中加入含有杂质的废弃物,记录所加废弃物与产生氢气的质量如下表所示。
次数 | 1 | 2 | 3 | 4 |
废弃物质量/g | 5 | 5 | 5 | 5 |
氢气质量/g | 0.15 | 0.15 | 0.1 | 0 |
请帮小组计算稀盐酸的溶质质量分数________。