题目内容
【题目】用元素符号或化学式填空:①4个铁原子________;②3个氧分子________;③2个铵根离子________;④水中氢元素的化合价为+1价________;⑤氢氧化铁________;⑥氯化镁中的阳离子________。
【答案】 4Fe 3O2 2NH4+ ![]() Fe(OH)3 Mg2+
Fe(OH)3 Mg2+
【解析】(1)铁原子直接用铁的元素符号表示,如表示多个原子,在元素符号前面加上数字,4个铁原子表示为4Fe;(2)氧分子是双原子分子,表示为O2 ,要表示3个氧分子,在前面加上3,表示为3O2 ; (3)铵根离子带1个单位的正电荷,1省略不写,要表示 2个铵根离子,在铵根离子前面加上2,表示为2NH4+;(4)表示某化合物中某元素的化合价,是在该元素的正上方标明,正负号在前,数字在后,水中氢元素的化合价为+1价表示为![]() ;(5)氢氧化铁中铁元素显+3价,化学式为Fe(OH)3;(6)氯化镁是由氯离子和镁离子构成,其中阳离子为Mg2+。
;(5)氢氧化铁中铁元素显+3价,化学式为Fe(OH)3;(6)氯化镁是由氯离子和镁离子构成,其中阳离子为Mg2+。

 轻松暑假总复习系列答案
轻松暑假总复习系列答案【题目】一些金属易生锈,某小组同学设计如下实验,对金属锈蚀进行探究.
【实验一】取5枚去油去锈的洁净铁钉,分别装入下表的试管中,进行实验.
实验图示 |
|
|
|
|
|
生锈时间 | 8min | 较长时间不生锈 | 5min | 3min | 1min |
(1)通过上述实验可知,温度越高铁钉生锈速率越____(填“慢”或“快”);在_____(填“酸性”、“碱性”或“中性”)环境中铁钉生锈速率较快.
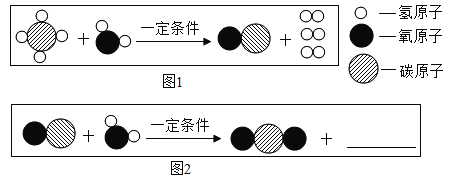
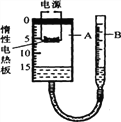
【实验二】为探究铁锈的成分,用图1所示装置(夹持仪器已省略)进行实验(每步反应和吸收均完全).
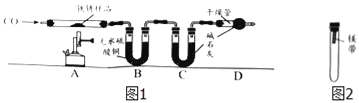
【查阅资料】无水硫酸铜能吸收水而变蓝,碱石灰既能吸收水也能吸收CO2.
(2)请指出图1所示实验装置的一个明显缺陷:___________________.
(3)加热前,先通入CO一段时间,目的是____________________.
(4)将铁锈样品加热,样品逐渐变黑,无水硫酸铜逐渐变蓝,由此推知铁锈中一定含有_____元素,从而推断出空气中的_______参加了铁生锈反应.
【实验记录】
铁锈样品的质量/g | 装置B的质量/g | 装置C的质量/g | |
反应前 | 23.2 | 232.4 | 198.2 |
反应后 | / | 239.6 | 211.4 |
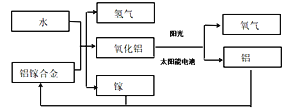
(5)根据上表数据推算,可确定铁锈的成分,用FexOynH2O表示,则n=_______;若缺少D装置,x:y的值_________(填“偏大”、“偏小”或“无影响”).
(6)欲通过实验探究镁带在空气中锈蚀的条件,用图2所示装置,试管内可选用的物质如下:
①O2 ②水 ③CO2 ④O2和CO2 ⑤CO2和水 ⑥O2和水 ⑦O2、CO2和水
至少需要选用___________(填数字序号),才能达到探究镁带锈蚀的条件.
(7)请写出镁带在空气中锈蚀,生成碱式碳酸镁[Mg3(OH)2(CO3)2]的化学方程式_______.