题目内容
【题目】一些金属易生锈,某小组同学设计如下实验,对金属锈蚀进行探究.
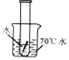
【实验一】取5枚去油去锈的洁净铁钉,分别装入下表的试管中,进行实验.
实验图示 |
|
|
|
|
|
生锈时间 | 8min | 较长时间不生锈 | 5min | 3min | 1min |
(1)通过上述实验可知,温度越高铁钉生锈速率越____(填“慢”或“快”);在_____(填“酸性”、“碱性”或“中性”)环境中铁钉生锈速率较快.
【实验二】为探究铁锈的成分,用图1所示装置(夹持仪器已省略)进行实验(每步反应和吸收均完全).
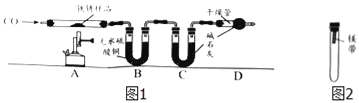
【查阅资料】无水硫酸铜能吸收水而变蓝,碱石灰既能吸收水也能吸收CO2.
(2)请指出图1所示实验装置的一个明显缺陷:___________________.
(3)加热前,先通入CO一段时间,目的是____________________.
(4)将铁锈样品加热,样品逐渐变黑,无水硫酸铜逐渐变蓝,由此推知铁锈中一定含有_____元素,从而推断出空气中的_______参加了铁生锈反应.
【实验记录】
铁锈样品的质量/g | 装置B的质量/g | 装置C的质量/g | |
反应前 | 23.2 | 232.4 | 198.2 |
反应后 | / | 239.6 | 211.4 |
(5)根据上表数据推算,可确定铁锈的成分,用FexOynH2O表示,则n=_______;若缺少D装置,x:y的值_________(填“偏大”、“偏小”或“无影响”).
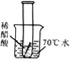
(6)欲通过实验探究镁带在空气中锈蚀的条件,用图2所示装置,试管内可选用的物质如下:
①O2 ②水 ③CO2 ④O2和CO2 ⑤CO2和水 ⑥O2和水 ⑦O2、CO2和水
至少需要选用___________(填数字序号),才能达到探究镁带锈蚀的条件.
(7)请写出镁带在空气中锈蚀,生成碱式碳酸镁[Mg3(OH)2(CO3)2]的化学方程式_______.
【答案】 快 酸性 没有进行尾气处理 排尽装置内的空气,防止发生爆炸 氢 水 4 偏小 ④⑤⑥⑦ 6Mg+3O2+4CO2+2H2O=2Mg3(OH)2(CO3)2
【解析】(1)对比实验1和实验4,实验3和实验5可知,温度越高铁钉生锈速率越快;对比实验1、2、3可知,铁钉在酸性环境中锈蚀较快; (2)尾气中含有有毒的一氧化碳气体,该装置中没有将其处理; (3)一氧化碳具有可燃性,不纯时加热或点燃易发生爆炸,所以先通入CO一段时间,排净装置内的空气;(4)无水硫酸铜能吸收水而变蓝,将铁锈样品加热,样品逐渐变黑,无水硫酸铜逐渐变蓝,这说明了反应后有水生成,说明铁锈中含有氢元素,也就是铁锈蚀的过程中有水参与; (5)硬质玻璃管内发生反应的化学方程式为:FexOynH2O+yCO![]() xFe+yCO2+nH2O,根据实验数据可知,反应中生成水的质量为:=7.2g,生成二氧化碳的质量为:=13.2g。设参加反应的CO的质量为w,则
xFe+yCO2+nH2O,根据实验数据可知,反应中生成水的质量为:=7.2g,生成二氧化碳的质量为:=13.2g。设参加反应的CO的质量为w,则
FexOynH2O+yCO![]() xFe+yCO2+nH2O
xFe+yCO2+nH2O
28y 44y
w 13.2g
![]()
w=8.4g
由质量守恒定律可知,生成铁的质量为:23.2g+8.4g﹣13.2g﹣7.2g=11.2g;
由于反应前后元素的种类与质量不变,所以23.2gFexOynH2O中含铁元素的质量为11.2g;含有“H2O”部分质量为7.2g;则余下的氧元素质量为:23.2g﹣11.2g﹣7.2g=4.8g
则:x:y:n=![]() :
:![]() :
:![]() =2:3:4,则FexOynH2O的化学式为Fe2O34H2O。
=2:3:4,则FexOynH2O的化学式为Fe2O34H2O。
D装置中的碱石灰既能吸收水也能吸收CO2,防止了空气中二氧化碳与水被装置C吸收而造成质量偏大,若没有装置D,则装置C因为吸收了空气中的水蒸气和二氧化碳而质量偏大,由此计算出的二氧化碳质量偏大,导致氧元素的质量偏大,x:y的值偏小;(6)通过实验探究镁带在空气中锈蚀的条件,应该选择这样几组实验:④O2和CO2;⑤CO2和水;⑥O2和水;⑦O2、CO2和水四组实验进行对比;(7)由镁带在空气中锈蚀,生成碱式碳酸镁[Mg3(OH)2(CO3)2]可以推测,是镁与氧气、水和二氧化碳反应生成了碱式碳酸镁6Mg+3O2+4CO2+2H2O=2Mg3(OH)2(CO3)2。

 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案【题目】分析处理图表中的信息是学习化学的一种重要方法,如表是NH4Cl和KNO3在不同温度时的溶解度数据:
温度/℃ | 10 | 30 | 50 | 70 | |
溶解度/g | NH4Cl | 33.3 | 41.4 | 50.4 | 55.2 |
KNO3 | 20.9 | 45.8 | 85.5 | 110 | |
根据上述数据,回答下列问题:
(1)从上表可知,50℃时,NH4Cl的溶解度为______g.
(2)NH4Cl和KNO3的溶解度受温度影响比较大的物质是________(填化学式).
(3)欲配制质量分数为10%的KNO3溶液,需要的玻璃仪器有烧杯、量筒、胶头滴管和________.
(4)烧杯中A中是60℃时,含有100g水的NH4Cl不饱和溶液,经过如图1的变化过程(在整个过程中,不考虑水分的蒸发),则C烧杯中溶液的质量为______g.
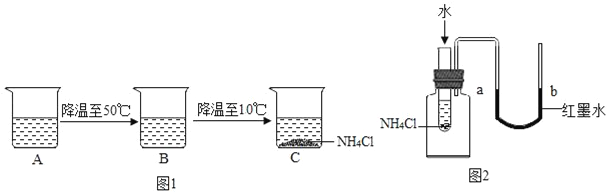
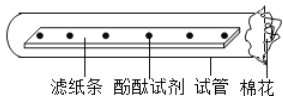
(5)某同学欲验证NH4Cl固体溶于水时吸收热量,设计如图2实验,通过观察到____现象得以验证.
A.a端液面高于b端液面
B.a端液面低于b端液面.
【题目】小华在吃黄花鱼时,看到其头骨上有两块白色的小石头。
[提出问题]这白色小石头中含有什么物质?
[查阅资料]小石头被称为“鱼脑石”,用来控制鱼在水中的沉浮。
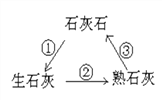
[猜想与假设]如图

[供选试剂] 10%稀盐酸,澄清石灰水,10%氢氧化钠溶液,紫色石蕊试液,酚酞试液。
[进行实验] 验证小力的猜想。
实验方法 | 可能看到的现象 | 结 论 |
①取粉碎后的“鱼脑石”加入_______ ②________ | ①_____________ ②______________ | _______ |
[反思] 如果实验证明了小力的猜想是正确的,你认为“鱼脑石”中一定含碳酸钙吗?简述理由。____________________________________________________。