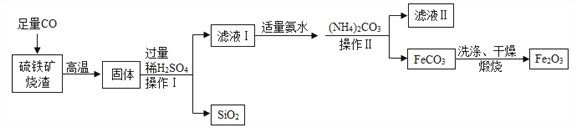
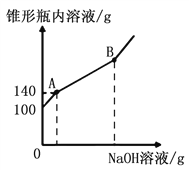
题目内容
【题目】80g质量分数为40%的氢氧化钠溶液与一定质量的氯化镁溶液混合,恰好完全反应,经过滤,得到滤液的质量为216.8g。请计算:
(1)原氯化镁溶液中溶质的质量分数;
(2)所得滤液中溶质的质量分数(计算结果精确至0.1%)。
【答案】23.8%, 21.6%
【解析】本题考查了溶质质量分数与化学方程式相结合的计算。
设:氯化镁的质量为x,生成氢氧化镁的质量为y,生成氯化钠的质量为z,
MgCl2+2NaOH═Mg(OH)2↓+2NaCl,
95 80 58 117
x 80g×40% y z
![]() x=38g,
x=38g,
![]() y=23.2g,
y=23.2g,
![]() z=46.8g,
z=46.8g,
氯化镁溶液的质量为:216.8g+23.2g-80g=160g,
原氯化镁溶液中溶质的质量分数为:![]() ×100%=23.8%,
×100%=23.8%,
所得滤液中溶质的质量分数为:![]() ×100%=21.6%。
×100%=21.6%。
答:(1)原氯化镁溶液中溶质的质量分数为23.8%;
(2)所得滤液中溶质的质量分数为21.6%。

 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案【题目】食盐(NaCl)、碳酸钠(Na2CO3)、生石灰(CaO)是制作皮蛋料泥的主要原料。制作料泥时,将上述原料加入适量水中,搅拌混合均匀即可。
(1)①制作料泥时,生石灰与水反应的化学方程式是__________________。
②制作料泥时,与碳酸钠反应的物质是_____________________(写化学式)。
(2)某化学兴趣小组对影响溶液碱性强弱的因素展开探究。用不同温度的水,配制溶质质量分数分别为2%、6%和10%的碳酸钠溶液,依次测量溶液的pH,记录数据如下表:
实验编号 | a1 | a2 | a3 | b1 | b2 | b3 | c1 | c2 | c3 |
溶质质量分数 | 2% | 2% | 2% | 6% | 6% | 6% | 10% | 10% | 10% |
水的温度(℃) | 20 | 40 | 60 | 20 | 50 | 60 | 20 | 50 | 70 |
溶液pH | 10.90 | 11.18 | 11.26 | 11.08 | 11.27 | 11.30 | 11.22 | X | 11.50 |
请你分析表中数据回答:
①溶液碱性最强的是___________(填实验编号)
②实验a1、b1、c1的实验目的是________________________。
③在相同的条件下,一定温度范围内,温度与碳酸钠溶液pH的关系是____________________。
④表格中X的数值可能是____________(填选项)。
A.11.20 B.11.25 C.11.37 D.11.62