题目内容
【题目】向lOOgBaCl2溶液中逐滴滴加Na2C03溶液,生成沉淀的质量与滴入Na2C03溶液的质量关系如图所示,请计算:
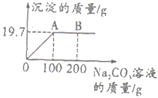
(1)生成沉淀的质量为_______________g。
(2)若在A点结束实验,过滤后所得溶液的溶质质量分数(计算结果精确到0.1%)。_________
【答案】 19.7 6.5%。
【解析】(1)根据图像解答;(2)根据生成碳酸钡沉淀的质量结合反应的化学方程式求出生成的氯化钠的质量,从而计算所得溶液的溶质质量分数。(1)由图可知,生成沉淀的质量为19.7g;(2)若在A点结束实验,设反应生成氯化钠的质量为x。
BaCl2+ Na2CO3=BaCO3↓+2NaCl
197 117
19.7g x
![]()
x=11.7g
过滤后所得溶液的溶质质量分数=![]() ×100%=6.5%
×100%=6.5%
答:若在A点结束实验,过滤后所得溶液的溶质质量分数6.5%。

 名校课堂系列答案
名校课堂系列答案【题目】实验室进行粗盐的提纯
(1)涉及的操作有:①过滤②溶解③蒸发结晶。正确的顺序是_________。(填序号)
(2)用托盘天平称量所需粗盐的质量,托盘天平调节平衡后,接下来的操作顺序
是_________(填序号)①在右盘中添加砝码,需要用游码时移动到相应刻度、②在托盘上分别放质量相等的纸、③在左盘中添加粗盐
(3)下图1中玻璃棒的作用是搅拌,_________。当_________时停止加热。
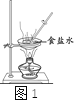
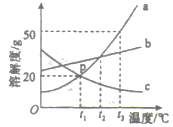
(4)配制溶液①用质量分数为5%的氯化钠溶液配制70g质量分数为3%的氯化钠溶液,需要水的质量是_____g。量取水的体积(水的密度为1g/mL),请在图2标出所需水的体积示数_________。②从表中找出稀释的过程需要用到的数据(20℃)是_______g/cm3。

20℃氯化钠溶液的密度
浓度% | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
密度g/cm3 | 1.005 | 1.013 | 1.02 | 1.027 | 1.034 | 1.041 | 1.043 |
【题目】如图的加热袋常用于野外加热食物。加热袋中的固体粉末含镁粉、铁粉和氯化钠,使用时向其中加入水袋中的水,即可产生大量热。实验小组针对放热过程中的反应原理展开探究。


【查阅资料】
常温下镁粉能与水发生置换反应,且放热。
【进行实验】
同学们用下图所示装置进行模拟实验:分别取不同成分的固体粉末放入甲中,通过分液漏斗向其中均加入8 mL水,读取甲中所得固液混合物的最高温度,实验记录如下表:
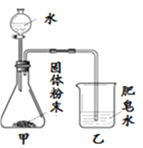
(实验时的室温为22.8℃)
实验序号 | A | B | C | D | E | F |
固体成分 | Mg | Fe | Mg+Fe | Mg+NaCl | Fe+NaCl | Mg+Fe+NaCl |
乙中现象 | 少量肥皂泡,难以点燃 | ______ | 少量肥皂泡,难以点燃 | 较多肥皂泡,点燃有爆鸣声 | 无肥皂泡 | 大量肥皂泡,点燃有爆鸣声 |
混合物温度 | 23.1℃ | 22.8℃ | 23.1℃ | 24.2℃ | 22.8℃ | 27.2℃ |
【解释与结论】
(1)实验B,乙中现象为_______________。
(2)实验A证明了镁粉与水能反应,完成该反应的化学方程式Mg+2H2O=____+H2 ![]() 。
。
(3)使镁粉与水迅速反应并放热的最佳方法是向镁粉中加入_____________。
【反思改进】
(4)同学们分析实验数据发现,升高的温度没有达到食品加热袋的效果,其可能的原因是___________。
(5)同学们根据实验结果进一步猜测,实验F中的反应结束后,甲中剩余固体混合物中仍然含有铁粉,检验其铁粉存在的的验方案为:取少量固体混合物________。
(6)从上述实验初步得出“NaCl溶于水没有热量的变化”的结论,依据的两个实验是(填实验序号)______________。