题目内容
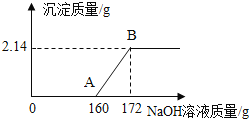
【题目】将氢氧化钠溶液慢慢滴入盛有稀盐酸的烧杯中,用温度计测量烧杯中溶液的温度,温度随加入将氢氧化钠溶液的质量变化曲线如图所示:
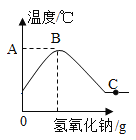
(1)在滴加的过程中,烧杯中溶液的pH如何变化?C点溶液中的溶质是什么?______
(2)由图可知,稀盐酸与氢氧化钠溶液发生的反应是吸热反应还是放热反应?______
【答案】从小于7逐渐变化到大于7,氢氧化钠和氯化钠 放热
【解析】
氢氧化钠和稀盐酸反应生成氯化钠和水。
(1)将氢氧化钠溶液慢慢滴入盛有稀盐酸的烧杯中,氢氧化钠和盐酸反应生成氯化钠和水,开始稀盐酸较多,pH小于7,随着反应的进行,pH逐渐增大,反应完全,pH等于7,继续滴加氢氧化钠溶液,pH大于7,故烧杯中溶液的pH从小于7逐渐变化到大于7,C点氢氧化钠过量,则C点溶液中溶质是过量氢氧化钠和生成的氯化钠。
(2)由图象中溶液温度的变化可知,随着反应的进行,温度逐渐升高,反应完全,温度降低,故稀盐酸与氢氧化钠溶液发生的反应是放热反应。

练习册系列答案
相关题目
【题目】关于下列事实的解释不正确的是( )
选项 | 事实 | 解释 |
A | 10mL酒精和10mL水混合后体积小于20mL | 分子之间有间隔 |
B | 稀硫酸和稀盐酸化学性质相似也存在差异 | 溶液中都含有H+ , 也存在不同的SO42-、Cl-离子 |
C | 酒精溶液不导电 | 溶液中没有自由移动的带电粒子 |
D | 化肥硫酸铵不能和熟石灰混放或混用 | 硫酸铵与熟石灰发生中和反应 |
A.A B.B C.C D.D