题目内容
一碳化学是以分子中只含有一个碳原子的化合物(如CO、CH4等)为原料来合成一系列化工原料和燃料的化学。CO是从煤的气化或合成气得到的。
(1)煤的气化的主要反应有:
①2C+O2==2CO ②C+H2O CO+H2 ③CO+H2O==CO2+H2
CO+H2 ③CO+H2O==CO2+H2
上述反应属于化合反应的是_______(填序号),属于氧化反应的是_______(填序号)。
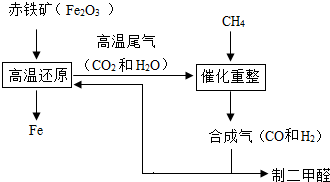
(2)合成气可通过天然气的重整得到,如CH4+H2O==CO+3H2。合成气可制二甲醚,二甲醚被称为21世纪的新型燃料。合成气还可用于冶炼金属,用它冶炼铁的部分生产过程示意如下:
(1)煤的气化的主要反应有:
①2C+O2==2CO ②C+H2O
 CO+H2 ③CO+H2O==CO2+H2
CO+H2 ③CO+H2O==CO2+H2上述反应属于化合反应的是_______(填序号),属于氧化反应的是_______(填序号)。
(2)合成气可通过天然气的重整得到,如CH4+H2O==CO+3H2。合成气可制二甲醚,二甲醚被称为21世纪的新型燃料。合成气还可用于冶炼金属,用它冶炼铁的部分生产过程示意如下:

①二甲醚(CH3OCH3)可由合成气(CO和H2)在一定的条件下制得。用合成气制二甲醚时,还产生了一种可参与大气循环的、常温下为液态的氧化物,写出该反应的化学方程式:___________________。
②合成气在冶炼铁的生产过程中所起的作用是_________________。
(3)某化学兴趣小组的同学为了测定某赤铁矿石中氧化铁的质量分数。
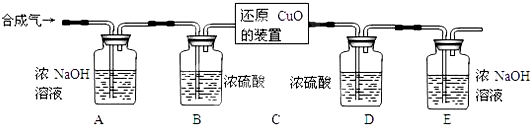
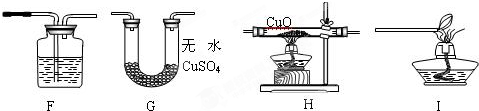
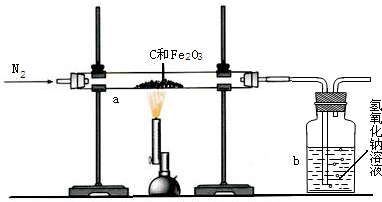
I.甲同学取一定质量的赤铁矿粉与过量的木炭粉混合后,用下图所示装置以合理的操作步骤测定(假设杂质始终不发生变化)。
②合成气在冶炼铁的生产过程中所起的作用是_________________。
(3)某化学兴趣小组的同学为了测定某赤铁矿石中氧化铁的质量分数。
I.甲同学取一定质量的赤铁矿粉与过量的木炭粉混合后,用下图所示装置以合理的操作步骤测定(假设杂质始终不发生变化)。

①实验中持续通入干燥的氮气。加热前就缓缓通入氮气一段时间,其作用是_______________。
②停止加热前是否需要先断开a和b的连接处以防止倒吸?为什么?__________________________。
③如果氢氧化钠溶液对二氧化碳的吸收是完全的,那么甲同学用氢氧化钠溶液的质量变化测定出氧化铁的质量分数将________(选填“偏大”、“偏小”或“准 确”),原因是________________。
Ⅱ.乙同学取矿石样品10g,加入足量稀盐酸,完全反应后,共用去稀盐酸109.5g,过滤得到滤渣2g(假设杂质既不溶于水也不与酸发生反应)。请你和乙同学一起计算赤铁矿石中氧化铁的质量分数和反应后 溶液中溶质的质量分数。(请写出计算过程)
②停止加热前是否需要先断开a和b的连接处以防止倒吸?为什么?__________________________。
③如果氢氧化钠溶液对二氧化碳的吸收是完全的,那么甲同学用氢氧化钠溶液的质量变化测定出氧化铁的质量分数将________(选填“偏大”、“偏小”或“准 确”),原因是________________。
Ⅱ.乙同学取矿石样品10g,加入足量稀盐酸,完全反应后,共用去稀盐酸109.5g,过滤得到滤渣2g(假设杂质既不溶于水也不与酸发生反应)。请你和乙同学一起计算赤铁矿石中氧化铁的质量分数和反应后 溶液中溶质的质量分数。(请写出计算过程)
(1)①;①②③
(2)①2CO+4H2 CH3OCH3+H2O
CH3OCH3+H2O
②将铁从铁矿石中还原出来(或作还原剂)
(3)I.①将装置内的空气排净
②不需要,因为实验中要持续通入氮气,直到反应完成后玻璃管内物质冷却,所以不会引起倒吸
③偏小;氢氧化钠溶液增重的质量由于一氧化碳的生成和气体带走的水蒸气而偏小(合理答案均给分)
Ⅱ.解:赤铁矿石中氧化铁的质量分数为: = 80%
= 80%
设反应生成氯化铁的质量为x。
Fe2O3+6HCl==2FeCl3+3H2O
160 325
8g x

x =16.25 g
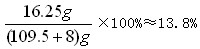
答:赤铁矿石中氧化铁的质量分数为80%,反应后溶液中溶质的质量分数约为13.8%。
(2)①2CO+4H2
 CH3OCH3+H2O
CH3OCH3+H2O②将铁从铁矿石中还原出来(或作还原剂)
(3)I.①将装置内的空气排净
②不需要,因为实验中要持续通入氮气,直到反应完成后玻璃管内物质冷却,所以不会引起倒吸
③偏小;氢氧化钠溶液增重的质量由于一氧化碳的生成和气体带走的水蒸气而偏小(合理答案均给分)
Ⅱ.解:赤铁矿石中氧化铁的质量分数为:
 = 80%
= 80%设反应生成氯化铁的质量为x。
Fe2O3+6HCl==2FeCl3+3H2O
160 325
8g x

x =16.25 g
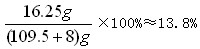
答:赤铁矿石中氧化铁的质量分数为80%,反应后溶液中溶质的质量分数约为13.8%。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 一碳化学是以分子中只含有一个碳原子的化合物(如CO、CH4等)为原料来合成一系列化工原料和燃料的化学.CO是从煤的气化或合成气得到的.煤的气化主要反应有:
一碳化学是以分子中只含有一个碳原子的化合物(如CO、CH4等)为原料来合成一系列化工原料和燃料的化学.CO是从煤的气化或合成气得到的.煤的气化主要反应有: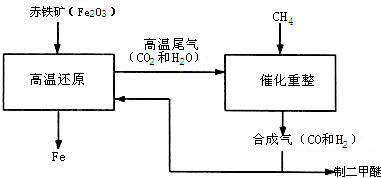
 (2011?仪征市一模)一碳化学是以分子中只含一个碳原子的化合物(如CO、CH4等)为原料来合成一系列化工原料和燃料的化学.工业上常用天然气和水蒸气或二氧化碳经高温催化反应得到CO和H2,得到的CO和H2的混合气被称为合成气.如图为利用合成气合成新型燃料二甲醚(CH3OCH3)及冶炼铁的部分生产过程.
(2011?仪征市一模)一碳化学是以分子中只含一个碳原子的化合物(如CO、CH4等)为原料来合成一系列化工原料和燃料的化学.工业上常用天然气和水蒸气或二氧化碳经高温催化反应得到CO和H2,得到的CO和H2的混合气被称为合成气.如图为利用合成气合成新型燃料二甲醚(CH3OCH3)及冶炼铁的部分生产过程. (1)利用高炉尾气中的水蒸气与甲烷催化重整得到合成气,化学方程式为
(1)利用高炉尾气中的水蒸气与甲烷催化重整得到合成气,化学方程式为