题目内容
【题目】化学兴趣小组的同学对“二氧化锰在过氧化氢分解前后的质量和化学性质没有改变”这一结论产生了兴趣,决定进行亲身验证.
(查阅资料)①过滤是将不溶于水的固体和液体分离开的操作,二氧化锰不溶于水.②在一定范围内,温度升高,化学反应的速率会加快。
(初步验证)小华提出先用电子天平称量1.0g的二氧化锰,然后将其与过氧化氢溶液中,请写出该反应的化学方程式______,待反应结束后,过滤,洗涤,再进行二次称量,结果发现所得数据大于1.0g,原因可是_______。
(实验改进)小强针对上述原因,提出烘干后再称量的方案,结果得到了准确的实验结论,与此同时,老师引导同学们可以尝试蒸发的方法,结果也得到了相同的结果.由此我们得出的实验结论是_____。
(深入探究)对于二氧化锰在反应前后化学性质没有改变的验证,小兵提出可以直接向刚蒸干的二氧化锰中滴入过氧化氢溶液,若能观察到仍有______的现象,就可以得出结论.但小芳对此产生了异议,她的理由是____。(已确认产生的气体为氧气)
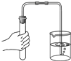
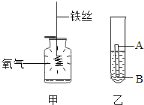
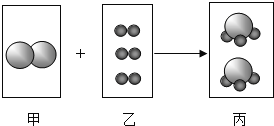
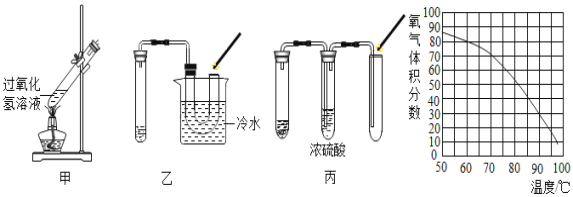
(实验反思)在过氧化氢制取氧气的过程中,二氧化锰的确起到了加快过氧化氢分解的作用,那么有没有别的方法也能起到这一效果呢?对此,兴趣小组的同学们展开了激烈的讨论,并最终设计出了如图甲所示的装置。
(1)此装置能较快收集到氧气的原因是________。
(2)课堂上同学们利用如图甲所示装置做功氧化氢制取氧气的实验时,用带火星的木条检验氧气,却发现带火星的木条很难复燃,这又是为什么呢?
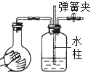
(3)针对这一异常现象,兴趣小组的同学们去请教了老师,老师在思考以后,决定对甲装置进行改进,如乙图所示,发现带火星的木条较易复燃(图中的加热装置已略去)。
(交流与讨论)
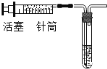
(4)兴趣小组的同学们受到启发,在查阅了相关资料后,又共同设计处了图丙所示的装置,发现带火星的木条也易复燃(图中的加热装置已略去),根据图乙装置的启示,请你分析浓硫酸的作用可能是_________。
(5)再加热过氧化氢溶液制取氧气的过程中,加热的温度与集气瓶中氧气的体积分数之间存在联系(如曲线图所示),若能使带火星的木条复燃所需的氧气的体积分数最低为49%(只考虑氧气的体积分数对实验结果的影响),现欲使带火星的木条复燃,应将加热过氧化氢溶液的最高温度控制在_________℃。
【答案】2H2O2![]() 2H2O+ O2↑ 没有干燥二氧化锰 二氧化锰在反应前后质量不变 产生大量气泡 刚蒸干的二氧化锰温度较高,能够加快过氧化氢的分解速率 在一定范围内,温度升高,化学反应的速率会加快 . 吸收水蒸气(或吸水或干燥氧气) 82或83
2H2O+ O2↑ 没有干燥二氧化锰 二氧化锰在反应前后质量不变 产生大量气泡 刚蒸干的二氧化锰温度较高,能够加快过氧化氢的分解速率 在一定范围内,温度升高,化学反应的速率会加快 . 吸收水蒸气(或吸水或干燥氧气) 82或83
【解析】
初步验证:
过氧化氢在二氧化锰催化作用下分解生成水和氧气,化学方程式为:2H2O2![]() 2H2O+ O2↑;待反应结束后,过滤,洗涤,再进行二次称量,结果发现所得数据大于1.0g,原因可能是没有干燥二氧化锰,导致二氧化锰表面附着了一定量的水;
2H2O+ O2↑;待反应结束后,过滤,洗涤,再进行二次称量,结果发现所得数据大于1.0g,原因可能是没有干燥二氧化锰,导致二氧化锰表面附着了一定量的水;
实验改进:
小强针对上述原因,提出烘干后再称量的方案,结果得到了准确的实验结论,与此同时,老师引导同学们可以尝试蒸发的方法,结果也得到了相同的结果,说明了二氧化锰在反应前后质量不变;
深入探究:
对于二氧化锰在反应前后化学性质没有改变的验证,小兵提出可以直接向刚蒸干的二氧化锰中滴入过氧化氢溶液,若能观察到仍然产生大量气泡,就可以得出结论,但小芳对此产生了异议,她的理由是:刚蒸干的二氧化锰温度较高,能够加快过氧化氢的分解速率;
实验反思:
(1)此装置能较快收集到氧气的理论依据是:在一定范围内,温度升高,化学反应的速率会加快;
(2)利用如图甲所示装置做过氧化氢制取氧气的实验时,用带火星的木条检验氧气,却发现带火星的木条很难复燃,这是因为此时氧气中混有大量水蒸气,很难使带火星的木条复燃;
交流与讨论:
(4)由图乙装置可知,冷水是为了降低温度使水蒸气液化,从而使氧气更纯净一些,因此浓硫酸的作用可能是吸收水蒸气(或吸水或干燥氧气);
(5)由图中可知,氧气的体积分数为49%时,温度约为81℃,因此欲使带火星的木条复燃,应将加热过氧化氢溶液的最高温度控制在82或83℃。