题目内容
【题目】下列叙述与对应的坐标图表示正确的是
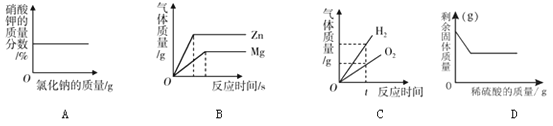
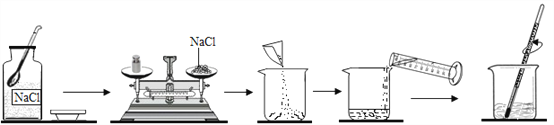
A. 向硝酸钾的饱和溶液中加入氯化钠
B. 将相同质量的Zn粉和Mg粉分别加入足量的稀盐酸中
C. 水的电解
D. 向一定量黄铜(铜锌合金)粉末中逐滴加入稀硫酸
【答案】D
【解析】A、向硝酸钾的饱和溶液中加入氯化钠时,氯化钠能够溶解,随着氯化钠的溶解,溶液质量增大,硝酸钾质量分数减小,错误; B、锌和稀盐酸反应生成氯化锌和氢气,镁和稀盐酸反应生成氯化镁和氢气,反应的化学方程式及其质量关系为:
Zn+2HCl═ZnCl2+H2↑,Mg+2HCl═MgCl2+H2↑,
65 2 24 2
由以上质量关系可知,由于镁和稀盐酸的反应速率比锌快,反应需要的时间短,并且完全反应后,镁和稀盐酸反应生成的氢气多,错误; C、电解水时,正极产生的是氧气,负极产生的是氢气,氧气和氢气的体积比约为1:2,质量比是8:1,错误; D、铜锌合金中只有锌能够和稀硫酸反应产生氢气,因此随着反应的进行固体逐渐减少,到锌反应完了,剩余的铜,质量保持不变,正确。故选D。

【题目】在实验探究课上,老师给了同学们一包红色粉末,该粉末是铜粉和氧化铁中的一种或两种。同学们为了确定该粉末的成分,进行如下探究,请你参与他们的探究并回答问题。
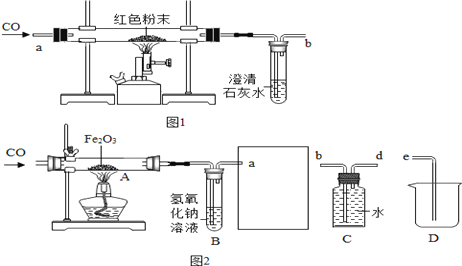
【猜想】猜想I:红色粉末是铜粉;猜想Ⅱ:红色粉末是氧化铁;猜想Ⅲ:红色粉末是______。
【实验】经过查阅资料、回忆已学过的知识,
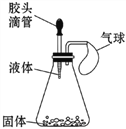
大家决定设计如图1所示的实验进行探究.请完成下列表格:
实验中可能出现的现象 | 结论 |
________________ | 猜想Ⅰ正确 |
红色粉末全部变为黑色,石灰水变浑浊 | 猜想Ⅱ正确 |
________________ | 猜想Ⅲ正确 |
【表达】通过实验及分析,确定红色粉末是铜粉和氧化铁的混合物,则在上述实验过程中一氧化碳和氧化铜所发生反应的化学方程式是_____________。
【反思】从环保角度看,图1所示的实验装置有不足之处,请说出其中一种改进方法:___________。
【拓展】为了进一步探究铁和铜的金属活动性强弱,你认为可选用下列试剂中的___(填序号)。
A.硝酸铜溶液 B.稀盐酸 C.氯化亚铁溶液 D.硫酸镁
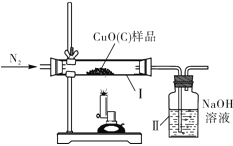
【应用】同学们用一氧化碳与氧化铁的反应来模拟炼铁的原理,装置如图2所示,请回答有关问题:
(1)B装置中氢氧化钠溶液的作用是__________________ 。
(2)为避免将CO排放到空气中,并回收利用CO,方框中连接的是C和D装置,导管接口的连接顺序应为a→_____→_____→______。(填字母)