题目内容
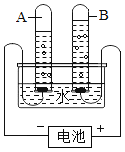
【题目】氢化钙(CaH2)常温下能与水反应生成H2,是野外工作人员便携燃料的来源。课外小组同学利用H2与金属钙反应制取CaH2(见图)
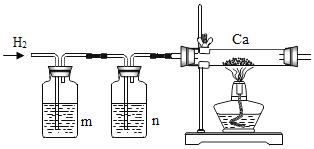
(1)反应所需H2可利用锌粒与稀盐酸反应制取,方程式为_____,该反应属于基本反应类型中的_____反应。
(2)洗气瓶中m、n应依次选择下列试剂的_____、_____(填序号)
A NaHCO3溶液 B NaOH溶液 C 浓硫酸
(3)为防止钙被氧化,在加热钙之前必须进行的操作是_____。
(4)CaH2与水反应的化学方程式为_____。氢气密度比空气_____(填“大”或“小”),试从微观探析角度解释其原因_____(已知同温同压下相同体积的任何气体都含有相同数目的分子)
(5)为防止空气中的二氧化碳、水蒸气与玻璃管中Ca或CaH2反应,在导管末端还应该连接一干燥管,所装试剂为_____。
【答案】Zn+2HCl=ZnCl2+H2↑ 置换 B C 先通入氢气 CaH2+2H2O=Ca(OH)2+2 H2↑ 小 氢分子比空气中的分子都小 碱石灰
【解析】
(1)锌和盐酸反应生成氯化锌和氢气,对应的化学方程式为:![]() ,由一种单质和一种化合物反应生成另一种单质和另一种化合物的反应是置换反应。
,由一种单质和一种化合物反应生成另一种单质和另一种化合物的反应是置换反应。
(2)由于生成的氢气中混有HCl和水蒸气,气体中含有多种杂质气体,应最后除去水蒸气,所以应该用氢氧化钠溶液先除去HCl,然后用浓硫酸干燥。所以洗气瓶中m、n应依次装入氢氧化钠溶液和浓硫酸。故填:B、C。
(3)为防止钙被氧化,即需要排空装置内的氧气,所以在加热钙之前必须进行的操作是先通入氢气。
(4)CaH2与水反应生成氢气,根据质量守恒定律可知,还生成氢氧化钙,对应的化学方程式为 ![]() ,氢气密度比空气小,是因为氢分子比空气中的分子都小。
,氢气密度比空气小,是因为氢分子比空气中的分子都小。
(5)为防止空气中的二氧化碳、水蒸气与玻璃管中Ca或CaH2反应,在导管末端还应该连接一干燥管,所装试剂为碱石灰,因为碱石灰既可以吸收二氧化碳也可以吸收水蒸气。

 阅读快车系列答案
阅读快车系列答案【题目】(1)水是生命的源泉,也是不可缺少的资源:
![]() 自然界的水常常遭到污染,污染物中氮和磷含量过高会造成水中藻类过度繁殖,使水质恶化,人们把这种现象称之为水质富营养化
自然界的水常常遭到污染,污染物中氮和磷含量过高会造成水中藻类过度繁殖,使水质恶化,人们把这种现象称之为水质富营养化![]() 这里的“氮和磷”是指______。
这里的“氮和磷”是指______。![]() 填字母
填字母![]()
A 元素B 原子C 离子D 分子
![]() 生活中,既能降低水的硬度,又能杀菌消毒的方法是______。
生活中,既能降低水的硬度,又能杀菌消毒的方法是______。
![]() 电解水的装置如图所示,管A、管B中的气体质量比是______。
电解水的装置如图所示,管A、管B中的气体质量比是______。
(2)除去下列物质中的杂质,所用试剂和操作方法正确的是_____(多选)。
选项 | 实验目的 | 实验方案 |
A | 除去NaCl溶液中的 | 加适量稀硫酸 |
B | 除去 | 将混合气体通入饱和NaHCO3溶液 |
C | 除去CaO中的 | 加水溶解,过滤 |
D | 除去 | 加适量的 |
【题目】依据下列60℃时的实验和数据完成下面小题。(已知:60℃时,NaCl和KNO3的溶解度分别为37.3g和110g)
| 序号 | ① | ② | ③ | ④ | ⑤ |
固体种类 | NaCl | NaCl | KNO3 | KNO3 | KNO3 | |
固体的质量/g | 30 | 60 | 30 | 90 | 120 | |
水的质量/g | 100 | 100 | 100 | 100 | 100 |
【1】①~⑤所得溶液属于饱和溶液的是
A. ①③B. ②④C. ②⑤D. ④⑤
【2】下列关于①~⑤所得溶液的说法不正确的是
A. 溶质质量:①<②B. 溶液质量:②<④
C. 溶质质量分数:①=③D. ⑤中溶质与溶剂的质量比为12:10