题目内容
2.氢气和氧气的混合气体37g,点燃充分反应生成水36g,则混合气体中氢气和氧气的质量比可能是( )| A. | 1:36 | B. | 2:35 | C. | 5:32 | D. | 4:33 |
分析 根据充分反应后生成36g水,利用化学反应方程式可知,4g氢气和32g氧气恰好完全反应生成36g水,则37g混合气体有剩余的气体存在,则有两种可能:①剩余气体为氢气;②剩余气体为氧气来分析解答.
解答 解:设参加反应反应的氢气和氧气的质量分别为x,y;
2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O
4 32 36
x y 36g
$\frac{4}{x}=\frac{32}{y}=\frac{36}{36g}$
x=4g
y=32g
①若剩余气体为氢气,则氢气的质量为4g+(37g-36g)=5g,即混合气体中有5g氢气和32g氧气;则氢气和氧气的质量比5:32;
②若剩余气体为氧气,则氧气的质量为32g+(37g-36g)=33g,即混合气体中有4g氢气和33g氧气,则氢气和氧气的质量比为4:33.
故选CD.
点评 本题考查学生利用化学反应方程式的计算来分析混合物的成分,学生应能利用化学反应判断恰好完全反应的量,要注意过量计算过程的思维训练.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
17.某课外兴趣小组的同学设计了如下三个实验来验证质量守恒定律:

实验Ⅰ:称量镁条,在空气中点燃,待反应结束后,将生成物全部收回再称量.
实验Ⅱ:将装有稀盐酸的小试管放入装有锌粒的烧杯中,称量,然后将盐酸与锌粒接触,过一会在称量.
实验Ⅲ:将装有氢氧化钠溶液的试管放入盛有硫酸铜的锥形瓶中,并在锥型瓶口塞上橡皮塞,称量,然后设法将两种溶液接触(有蓝色氢氧化铜沉淀和硫酸钠生成)
过一会再称量.数据见表:
(1)在实验Ⅰ中,反应后的质量比反应前明显增加,请用质量守恒定律加以解释反应后生成的氧化镁的质量等于反应的镁的质量和反应的氧气质量的和.
(2)实验Ⅱ中发生反应的化学方程式为Zn+2HCl=ZnCl2+H2↑.
(3)这三个实验中,实验Ⅲ正确反映了反应物与生成物之间的质量关系.请从分子、原子的角度解释反应前后质量相等的原因反应前后,原子种类不变,原子总个数不变,原子的质量不变.
(4)实验Ⅰ、Ⅱ不能正确反映反应物和生成物之间的质量关系,选一例说明实验设计中的不当之处,并提出改进思路实验Ⅱ中,不当之处是反应装置是敞开的;应该改进为:把锌粒和稀盐酸放在密闭容器中.

实验Ⅰ:称量镁条,在空气中点燃,待反应结束后,将生成物全部收回再称量.
实验Ⅱ:将装有稀盐酸的小试管放入装有锌粒的烧杯中,称量,然后将盐酸与锌粒接触,过一会在称量.
实验Ⅲ:将装有氢氧化钠溶液的试管放入盛有硫酸铜的锥形瓶中,并在锥型瓶口塞上橡皮塞,称量,然后设法将两种溶液接触(有蓝色氢氧化铜沉淀和硫酸钠生成)
过一会再称量.数据见表:
| 编号 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
| 反应前/g | 4.8 | 112.6 | 118.4 |
| 反应后/g | 8.0 | 112.4 | 118.4 |
(2)实验Ⅱ中发生反应的化学方程式为Zn+2HCl=ZnCl2+H2↑.
(3)这三个实验中,实验Ⅲ正确反映了反应物与生成物之间的质量关系.请从分子、原子的角度解释反应前后质量相等的原因反应前后,原子种类不变,原子总个数不变,原子的质量不变.
(4)实验Ⅰ、Ⅱ不能正确反映反应物和生成物之间的质量关系,选一例说明实验设计中的不当之处,并提出改进思路实验Ⅱ中,不当之处是反应装置是敞开的;应该改进为:把锌粒和稀盐酸放在密闭容器中.
11.下列物质依据氯元素化合价规律排列,次序为KC1、HClO、( )、KClO3、HClO4,则空格内的物质应是( )
| A. | NaCl | B. | C1O2 | C. | Cl2 | D. | HC1O3 |
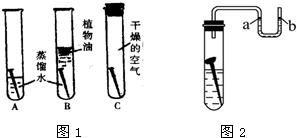
 在“空气中氧气含量的测定”实验探究中,小涵设计了如下实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.(实验装置如图所示)回答下列问题:
在“空气中氧气含量的测定”实验探究中,小涵设计了如下实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.(实验装置如图所示)回答下列问题: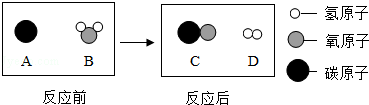
 人的胃液里含有适量的盐酸,可以帮助消化,但如果胃酸分泌过多,人会感到胃痛.小军拿来了一种抗酸药(治疗胃酸过多的药物),该药物说明书的部分内容如图所示.
人的胃液里含有适量的盐酸,可以帮助消化,但如果胃酸分泌过多,人会感到胃痛.小军拿来了一种抗酸药(治疗胃酸过多的药物),该药物说明书的部分内容如图所示.