题目内容
【题目】盐酸是一种广泛应用于入们生活、生产中的重要物质。在实验课上,化学兴趣小组的同学进行了与盐酸有关的探究。
[探究一]稀盐酸的化学性质
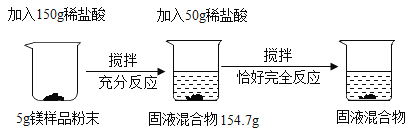
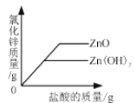
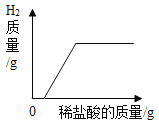
实验1:小组同学进行了如图1所示的实验。

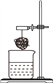
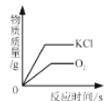
实验中观察到甲试管中有气泡产生,用图2所示装置收集产生的气体,检验气体已收集满的方法是_______。
乙试管中无明显现象,于是继续进行探究。
[探究二]乙试管中是否发生了化学反应?
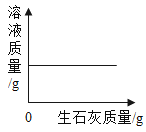
实验2:小组同学取少量实验后乙试管中的溶液于另一试管中,滴入几滴酚酞溶液,观察到_____,证明稀盐酸和石灰水发生了反应。
稀盐酸和石灰水反应的化学方程式为_______。
[探究三]混合后废液中的溶质成分。
小组同学将实验1中甲、乙两个实验后的废液倒入同一个洁净的烧杯中,观察到先有气泡产生,后有白色沉淀出现。将烧杯中的混合物过滤,得到滤渣和滤液。
[提出问题]滤液中溶质的成分是什么?
[作出猜想]猜想一:只有NaCl 猜想二:_________ 猜想三:NaCl和Na2CO3
[进行实验]实验3:取少量滤液于试管中,向其中滴加_________,无明显现象,证明猜想二不正确。
实验4:另取滤液,_______(填实验方案),证明猜想三成立。
[拓展应用]如果在实验1的甲试管中加入过量稀盐酸,所得到的溶液,无须另加试剂,只要对溶液进行__________(填操作名称),即可从中得到NaCl固体。
【答案】将燃着的小木条放在导管口b处,小木条熄灭 溶液呈无色 ![]() NaC1和CaCl2 Na2CO3溶液(合理即可) 用pH试纸测定其pH> 7(合理即可) 蒸发结晶
NaC1和CaCl2 Na2CO3溶液(合理即可) 用pH试纸测定其pH> 7(合理即可) 蒸发结晶
【解析】
[探究一]
实验1:碳酸钠和稀盐酸反应生成氯化钠、二氧化碳、水,实验中观察到甲试管中有气泡产生,用图20所示装置收集产生的二氧化碳气体,二氧化碳的密度大于空气,从a端进入,检验气体已收集满的方法是将燃着的小木条放在导管口b处,小木条熄灭。
[探究二]
实验2:小组同学取少量实验后乙试管中的溶液于另一试管中,滴入几滴酚酞溶液,观察到溶液呈无色,说明氢氧化钙已经完全反应,证明稀盐酸和石灰水发生了反应。
稀盐酸和石灰水反应生成氯化钙和水,反应的化学方程式为![]() 。
。
[探究三]
小组同学将实验1中甲、乙两个实验后的废液倒入同一个洁净的烧杯中,观察到先有气泡产生,后有白色沉淀出现。说明滤液中一定没有氯化氢,将烧杯中的混合物过滤,得到滤渣和滤液。
[提出问题]
滤液中溶质的成分是什么?
[作出猜想]
猜想一:只有NaCl 猜想二: NaC1和CaCl2 猜想三:NaCl和Na2CO3
[进行实验]
实验3:取少量滤液于试管中,向其中滴加Na2CO3溶液,无明显现象,证明猜想二不正确。
实验4:另取滤液,用pH试纸测定其pH> 7,证明猜想三成立。
[拓展应用]
如果在实验1的甲试管中加入过量稀盐酸,所得到的溶液,无须另加试剂,只要对溶液进行蒸发结晶即可从中得到NaCl固体。

【题目】如图为干电池的结构示意图,请利用所学知识完成下列问题。
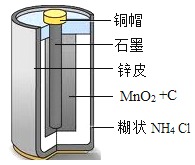
(l)碳棒(主要成分是石墨)可用作干电池的电极,说明石墨具有_____性。
(2)把 NH4Cl配制成溶液,并结合如表填空。
溶液 | K2SO4溶液 | NH4Cl溶液 | 氨水 | K2CO3溶液 |
加入紫色石蕊溶液 | 紫色 | 红色 | 蓝色 | 蓝色 |
①通过观察如表可知,NH4Cl溶液的 pH_____(填“>”“<”或者“=”)7。
②表中属于碱性氮肥的是_____。
(3)干电池中用到了铜和锌两种金属,请你写出一种证明两种金属活动性强弱的方案_____。
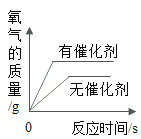
(4)干电池的材料很多可以回收利用。例如:回收的二氧化锰在实验室制取氧气时,所起的作用_____;干电池中的锌壳可以回收用于实验室制取氢气,反应的化学方程式为_____。