题目内容
【题目】a、b、c三种物质的溶解度曲线如图3所示,下列说法正确的是
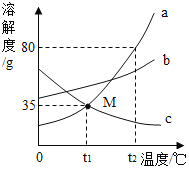
A.t1°C时a与c溶液的溶质质量分数相等
B.降温可以使c的不饱和溶液变为饱和溶液
C.b中含有少量a,可以用蒸发结晶的方法提纯b
D.t2°C时,a的饱和溶液溶质质量分数为80%
【答案】C
【解析】
A、t1°C时,a与c的溶解度相同,根据饱和溶液中溶质质量分数=![]() ,a与c饱和溶液的溶质质量分数相等,故错误;
,a与c饱和溶液的溶质质量分数相等,故错误;
B、C物质的溶解度随温度的升高而增大,降温不可以使c的不饱和溶液变为饱和溶液,故错误;
C、b的溶解度受温度影响较小,b中含有少量a,可以用蒸发结晶的方法提纯,故正确;
D、t2°C时,a的溶解度为80g,a饱和溶液溶质质量分数为:![]() 80%,故错误;
80%,故错误;
故选:C。

 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案【题目】溶解度是我们初中化学常见的概念,请回答下列问题。
I.下表是NaC1、KNO3在不同温度下的溶解度:
温度/℃ | 0 | 20 | 40 | 60 | 80 | |
溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | |
(1)要比较NaC1、KNO3在水中的溶解能力,需要控制的变量是水的质量和_____________________。
(2)从KNO3溶液中获取其晶体适宜的方法是_____________________。
(3)20℃时,各取NaC1、KNO3固体3.5g加入10g水中,充分溶解后达到饱和状态的是___溶液。
(4)若将上述数据在坐标中绘制成NaCl、KNO3的溶解度曲线,两条曲线的交,点对应的温度范围是(_____)
A 0°C~20°C
B 20°C ~40°C
C 40°C ~60°C
D 60°C ~80°C
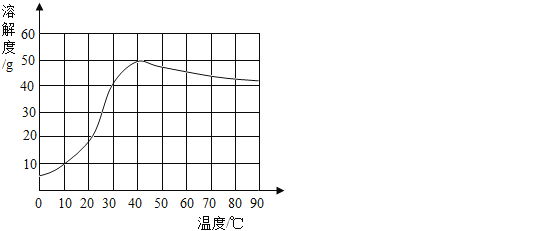
II.将质量为30g的B物质加入到50g水中,充分搅拌后,剩余物质的质量随温度的关系如图所示,过程中不考虑水分蒸发,回答问题:

(5)固体B的溶解度随温度的升高而____________(填“增大”或“减小”) 。
(6) t1℃时,B的溶解度是___________。