题目内容
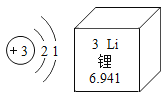
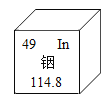
【题目】下表为元素周期表中部分元素的相关信息,请回答相关问题。
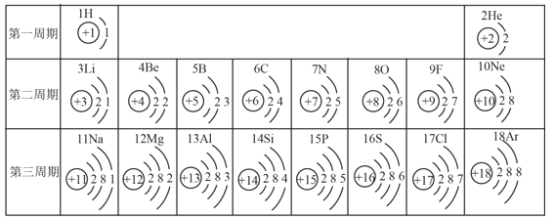
(1)利用表中所给的元素,写出具有10个电子的常见的分子、阳离子和阴离子的符号各一个:分子___,阳离子___,阴离子___。
(2)请从结构和性质的关系角度,解释为什么He和Ne最外层电子数不同,但化学性质相似,均比较稳定___。
【答案】H2O(NH3、CH4、HF 均可) Na+(Mg2+、Al3+、NH4+ 均可) F-(OH-、O2-、N3-均可) 最外层电子数决定了元素的化学性质,最外层电子数全满,元素化学性质稳定;He 最 外层为第一层,有 2 电子,Ne 最外层为第二层,有 8 电子,均为全满结构,故性质相似,均比较稳定。
【解析】
(1)1个水分子中含有1个氧原子和2个氢原子,1个氧原子有8个质子,1个氢原子中有1个质子,1个水分子中含有质子数=8+1×2=10,水分子呈电中性,所以1个水分子中含有10个电子,10个电子的常见的分子有水分子、甲烷分子、氨分子、氟化氢分子等,化学式分别为H2O、NH3、CH4、HF;具有10个电子阳离子有钠离子或镁离子或铝离子以及铵根离子等,离子符号分别为Na+、Mg2+、Al3+ 、NH4+;具有10个电子阴离子有氧离子、氟离子、氢氧根离子、氮离子,离子符号分别为O2-、F-、OH-、N3-等;
(2)最外层电子数决定了元素的化学性质,最外层电子数全满,元素化学性质稳定;He 最 外层为第一层,有 2 电子,Ne 最外层为第二层,有 8 电子,均为全满结构,性质相似,均比较稳定。

练习册系列答案
相关题目