题目内容
【题目】下图是硝酸钾和氯化钠的溶解度曲线。

(1)两种物质中,溶解度受温度影响较小的是__________。
(2)使接近饱和的氯化钠溶液变为饱和溶液的一种方法是________。
(3)60℃时,硝酸钾饱和溶液中溶有少量的氯化钠,提纯硝酸钾应采用的方法是________。
【答案】氯化钠 加溶质或蒸发溶剂或降低温度 降温结晶
【解析】
(1)由溶解度曲线可知:两种物质中,溶解度受温度影响较小的是氯化钠;故答案为:氯化钠;
(2)使接近饱和的氯化钠溶液变为饱和溶液的一种方法是:加溶质或蒸发溶剂或降低温度;故答案为:加溶质或蒸发溶剂或降低温度;
(3)60℃时,硝酸钾饱和溶液中溶有少量的氯化钠,提纯硝酸钾应采用的方法是:降温结晶,因为硝酸钾的溶解度随温度的升高变化比氯化钠大;故答案为:降温结晶.

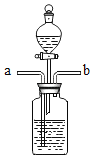
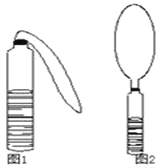
【题目】(1)小杰在一个玻璃瓶中装了半瓶液体,从另一个玻璃瓶中用镊子取出了一些固体颗粒,他把固体的小颗粒用镊子投入瓶中,立即将瘪气球的开口端套住瓶口,再用橡皮筋拉紧,如图1所示,不久,大家看到气球膨胀起来了,如图2,要产生这种现象,则可能的物质组合是:
液体 | 固体 | |
可能1 | _____ | _____ |
可能2 | _____ | _____ |
(2)小明在塑料瓶里装了液体后,充入了一种气体,立即拧紧瓶盖,一会儿,瓶子变瘪了,如图2,要产生这种现象,则可能的物质组合是:
液体 | 固体 | |
可能1 | _____ | _____ |
可能2 | _____ | _____ |
【题目】在小英家的仓库里,堆放着一袋袋化肥——碳酸氢铵(NH4HCO3)。过了一个夏天,小英发现这种化肥所持有的刺激性气味变得更浓烈了,有些化肥袋里碳酸氢铵变少了,检查发现变少的化肥包装袋没有密封,化肥没有撒落在地上,也没有人进过仓库打开使用。为了探究这些化肥减少的原因,小英在实验室取了一些碳酸氢铵粉末,放在蒸发皿中加热,过一会儿观察到粉末完全消失,同时也闻到了这种刺激性气味。粉末为什么会消失呢?
(提出问题)碳酸氢铵粉末消失的原因是什么?
(猜想)①碳酸氢铵粉末在不加热或加热条件下由固态变成它的气态。
②碳酸氢铵在不加热或加热条件下发生分解反应,可能产生的物质有氨气和一些氧化物。
(查阅资料)①碳酸氢铵属于氮肥,不具有升华的性质,说明上述猜想_____(填序号)不成立;②氨气(化学式NH3)具有特殊的刺激性气味,极易溶于水,其水溶液呈碱性,但干燥的氨气不能使干燥的红色石蕊试纸变蓝;③NO2为红棕色气体。NO为无色气体,在空气中易发生反应:2NO+O2===2NO2 。
(实验操作,现象与结论)
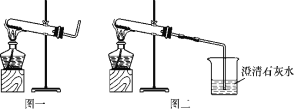
实验操作 | 实验现象 | 实验结论 |
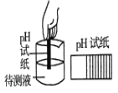
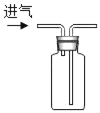
①取适量碳酸氢铵于试管中加热,如图一所示,将干燥的红色石蕊试纸接近导管口 | 产生强烈的刺激性气味,试管壁上有无色液滴且试纸变蓝,但未见红棕色气体 | 分解产物中有____和__,没有________________。 |
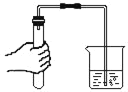
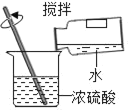
②按如图二所示装置继续实验,直到反应完全 | 澄清石灰水变浑浊 | 分解产物有___________。 |
(拓展应用)
①请写出碳酸氢铵发生分解反应的化学方程式____________。
②写出图二中澄清石灰水变浑浊的化学方程式_____________。
③判断:碳酸氢铵是否可用于实验室制取氨气?_______说明理由
④如果你家里有碳酸氢铵化肥,你应该如何保存?______________________。