题目内容
【题目】衢州某地有丰富的石灰石资源。科学兴趣小组的同学欲测定该地石灰石的纯度,进行了如下的实验:取50克稀盐酸,等分成4份。将石灰石样品放烧杯中,然后分四次加入分好的稀盐酸,每次充分反应后都放在电子天平上称量,并将读数记录在表格中。![]() 假设样品中的杂质不溶于水也不与盐酸反应,不计水分散失和盐酸的挥发
假设样品中的杂质不溶于水也不与盐酸反应,不计水分散失和盐酸的挥发![]()
空烧杯 | 加入 样品后 | 第一次加 入盐酸后 | 第二次加 入盐酸后 | 第三次加 入盐酸后 | 第四次加 入盐酸后 | |
读数(g) | 32.6 | 42.6 | 54.22 | 65.84 | 77.46 | 89.3 |
(1)根据记录的数据可知,反应生成的二氧化碳的质量为______克。
(2)石灰石中碳酸钙的质量分数为___________?
【答案】3.3g 75%
【解析】
(1)由表可知,第四次加入稀盐酸后,碳酸钙完全反应,故生成二氧化碳的质量为:
42.6g+50g-89.3g=3.3g
(2)设生成3.3g二氧化碳需要碳酸钙的质量为x。
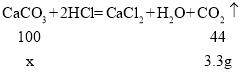
![]() 解得x=7.5g
解得x=7.5g
石灰石中碳酸钙的质量分数为:![]() ×100%=75%
×100%=75%
答:石灰石中碳酸钙的质量分数为75%。
故答案为:
(1)3.3g;
(2)75%。

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
【题目】在一只密闭容器内有四种物质,在一定条件下充分反应,测得反应前后各物质的质量如表:
物质 | X | Y | Z | Q |
反应前质量/g | 8 | 2 | 40 | 5 |
反应后质量/g | 待测 | 24 | 8 | 23 |
下列说法不正确的是( )
A. 其中X、Z为反应物B. 反应后生成Y、Q的质量比为24:23
C. 反应后X的质量为0D. 其中Y和Q为生成物