��Ŀ����
����Ŀ��Һ��ʯ�����Ǽ�ͥ����ȼ�ϣ���Ҫ�ɷ��DZ���Ͷ��飮
���� ���� | �۵�/�� | �е�/�� | ȼ�շ�Ӧ |
���� | ��189.7 | ��42.1 | C3H8+5O2 |
���� | ��138.4 | ��0.5 | 2C4H10+13O2 |
��1�����ϱ����Ϸ���������Ͷ�������������ǣ����³�ѹ�³�_____̬�����������Һ���̡�������ѧ�����ǣ�����_____ �ԣ�
��2��Һ��ʯ����ȼ����Ҫ���������������ݻ�ѧ����ʽ���㣺59g������ȼ������Ҫ������������_____��
��3����֪��̼����ĺ�����Խ�ߣ���ͬ�����³��ȼ��ʱ����CO2��Խ�٣� �Ƚϼ��顢����Ͷ���������������������������ྻ��ȼ����_____���ѧʽ����
��4������ȼ�Ͼ��м�����ʹ�÷�����ŵ㣬��ʹ��ʱӦ�ر�ע�ⰲȫ���⣮
��������ϵķ����ڲ��ã�������Ӧ���㣬ȼ�ղ���֣�������_____��_____��
����ˮ������ʱ���˲�ҪԶ����ߣ��������Ϩ�����û�м�ʱ�ر�ȼ�����ȼ��������ڳ�������ɢ��������ᷢ��_____��Σ�գ�
���𰸡����� ��ȼ�� 211.6g CH4 �����к�����CO, ʹ���ж����˷�ȼ�ϣ� ��ը
��������
��1��������Ŀ��������Ϣ���н��
��2�����û�ѧ����ʽ���ݶ���������������������������
��3�����ݼ��顢����Ͷ�����ӵĻ�ѧʽ���ԱȽ��������������
��4�����ݺ�̼���岻��ȫȼ�յIJ�����н���Լ���ȼ�����岻���ᷢ����ը���н��
��𣺽⣺��1������Ͷ���ķе�Ϊ-42.1����-0.5�������Գ��³�ѹ�³���̬����Ϊ����Ͷ��鶼�ܺ�������Ӧ���ɶ�����̼��ˮ���������ǵĻ�ѧ�����Ƕ����п�ȼ�ԣ�
��2����59g������ȼ������Ҫ������������Ϊx��
2C4H10+13O2![]() 8CO2+10H2O
8CO2+10H2O
116 416
59g x
![]()
x=211.6g
��59g������ȼ������Ҫ������������Ϊ211.6g��
��3�����Խ����顢���顢����Ļ�ѧʽCH4��C3H8��C4H10��ת��ΪC12H48��C12H32��C12H30����̼ԭ�Ӹ�����ͬ����ԭ�����������������ҲҪԽ�����Լ�������ྻ��ȼ�ϣ�
��4������̼�����ȼ�����ڿ�����Ӧ���㣬ȼ�ղ���֣�������һ����̼����һ����̼�ж�������������ϵķ����ڲ��ã�������Ӧ���㣬ȼ�ղ���֣�������ú���ж��Լ��˷�ȼ�ϣ������ڿ�ȼ�����岻����������ᷢ����ը��
�ʴ�Ϊ����1��������ȼ����2��211.6g����3��CH4����4�������к�����CO,ʹ���ж����˷�ȼ�ϣ���ը��

 �ƸԴ��ž�ϵ�д�
�ƸԴ��ž�ϵ�д�����Ŀ���±�ΪijʳƷ��װ���IJ���˵������ش��������⣺
��Ʒ���� | XX���� |
���� | С��ۡ�ֲ���͡��ʼ�����ʳ�Ρ����ɼ���ʳ���㾫�� |
��� | 500g |
���淽�� | ������������ﴦ����������ֱ�� |
������ | 270�� |
��1�������м��뼦�����ж����������á������Ը��Ʊ��ɵĿڸв�ʹ������һ���������Եȣ���Ӫ���ĽǶȿ���������������______��
��2�������п����������߲˵�������______��
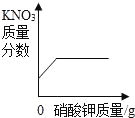
��3��С����и������ۣ��仯ѧʽ�ɱ�ʾΪ��C6H10O5��n����6.48�˵����������ھ���һϵ�еı仯����ת��Ϊˮ��______�˶�����̼��
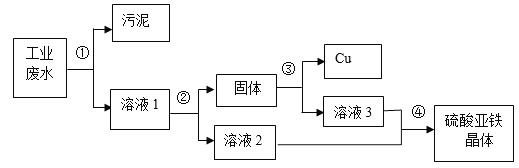
����Ŀ������ͼ��������ʵ��������ǣ�������
A | B | C | D |
��һ����п���м������ϡ���� | ��һ�����Ȼ�隣�����Һ�в��ϼ���ˮ | t��ʱ����һ���������͵��������Һ�в��ϼ�������ؾ��� | ��һ�����������ƺ����������Ļ����Һ�м���ϡ���� |
|
|
|
|
A. AB. BC. CD. D
����Ŀ���������ᩁ����������BaCl2��ų��ж�����H2S����ˮ��Һ�����ԣ�������NaOH��Һ����H2S��ȡNa2S�������ֳƳ�����մƼ�����з�Ӧ�Ļ�ѧ����ʽΪ��H2S+2NaOH��Na2S+2H2O
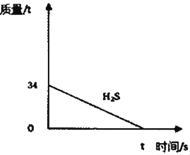
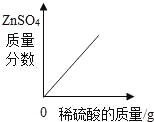
��1����ij������ÿ��Ҫ����34��H2S������������������Һ�е�����NaOH���ٶ�_____����д��������̣�
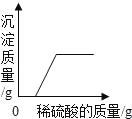
��2����ͼ�Ѿ���������34��H2S�������仯���ߣ�����ͼ�л���������Na2S�����ı仯���ߣ������������ϱ�����Ӧ������_____��
��3�������ǻ���H2S���յĸ��������ɱ���
��Ŀ | ���ۣ���Ԫ/�֣� |
NaOH | 0.25 |
Na2S | 0.5 |
�������ã��Դ���1��H2S�ƣ� | 0.12 |
��ҵ����β���迼�Ǿ���Ч������Ч�棬�����������Ϸ��������Ӿ���Ч�濼�����ִ���34��H2S�ķ�����ӯ��_____��Ԫ��
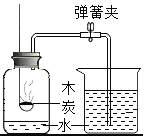
����Ŀ������ʵ����Ʋ��ܴﵽʵ��Ŀ���ǣ�������
ѡ�� | A | B | C | D |
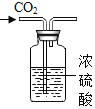
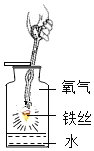
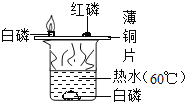
ʵ�� Ŀ�� | ���������̼ | ��֤��˿���� ������ȼ�� | �ⶨ������ �������� | ̽����ȼ�� ȼ������ |
ʵ�� ���� |
|
|
|
|
A. AB. BC. CD. D