题目内容
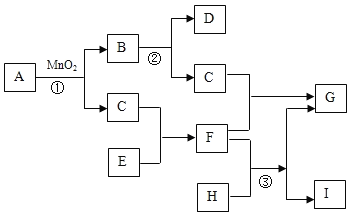
【题目】某兴趣小组的同学们利用老师提供的稀硫酸、碳酸钾、硫酸铜、氯化钡、氢氧化钾五种溶液,进行“酸、碱、盐”之间是否发生反应”的探究活动,活动结束后,将废液都倒入同一废液缸中,废液呈浑浊状态。为了验证废液的成分,先加入适量酚酞溶液,再按以下流程将浑浊的废液进行处理(注:![]() 溶液呈碱性);
溶液呈碱性);
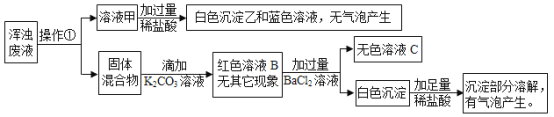
请回答下列问题:
(1)操作①的名称是________。
(2)沉淀甲中含有的物质是________。
(3)将足量稀盐酸加入到沉淀丙中,写出有气体生成的反应化学方程式________。
(4)加入![]() 溶液的目的是________。无色溶液A中一定含有的溶质是________。
溶液的目的是________。无色溶液A中一定含有的溶质是________。
【答案】过滤 硫酸钡、氢氧化铜 BaCO3+2HCl=BaCl2+H2O+CO2↑ 检验B中是否含有硫酸根离子 硫酸钾和氯化钾
【解析】
沉淀甲中加入稀盐酸,得到沉淀乙和蓝色溶液,无气泡产生,所以乙是硫酸钡沉淀,所以沉淀甲中含有氢氧化铜沉淀,蓝色溶液是氯化铜,沉淀甲中不含碳酸钡沉淀,白色沉淀丙中加入稀盐酸,沉淀部分溶解,有气泡产生,所以丙中一定含有碳酸钡和硫酸钡,所以溶液B中含有碳酸钾和硫酸钾,经过验证,推导正确。
由分析可知:
(1)过滤可以将不溶性固体从溶液中分离出来,所以操作①的名称是过滤;
(2)通过推导可知,沉淀甲中含有的物质是:硫酸钡、氢氧化铜;
(3)将足量稀盐酸加入到沉淀丙中,有气体生成的反应是碳酸钡和盐酸反应生成氯化钡、水和二氧化碳,化学方程式为:BaCO3+2HCl=BaCl2+H2O+CO2↑;
(4)加入BaCl2溶液的目的是:检验B中是否含有硫酸根离子,无色溶液A中一定含有的溶质是硫酸钾和氯化钾。

 教学练新同步练习系列答案
教学练新同步练习系列答案【题目】石灰石样品的主要成分是碳酸钙(已知其它杂质不与稀盐酸反应)。课外小组同学将50g稀盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象:
次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
加入稀盐酸的质量/g | 10 | 10 | 10 | 10 | 10 |
剩余固体的质量/g | 16 | 12 | 8 | 4 | m |
请计算:
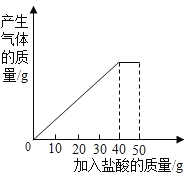
(1)m的值是______g.
(2)该样品中碳酸钙的质量分数为_________。
(3)求反应过程中产生二氧化碳的质量_________。(写出计算过程)