题目内容
【题目】请根据下图回答问题:
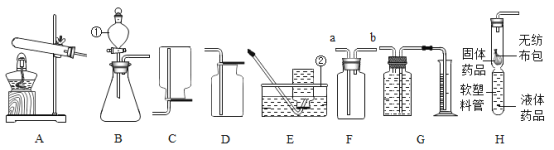
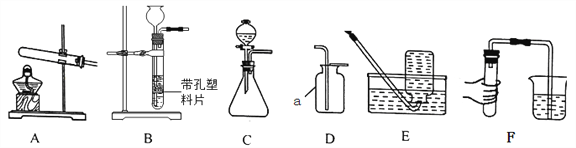
(1)写出标有序号仪器的名称:①_____;②_____;
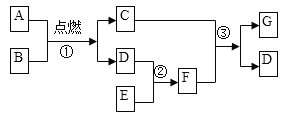
(2)A、E组合装置制取氧气,她按操作规范检查了装置的气密性,发现气密性良好,但在加热过程中E装置内导管口始终没有气泡冒出,其可能原因是_____;若制得的氧气不纯,可能的原因是_____;
(3)装置B是常用的氧气发生装置,其突出优点是_____。装置H是用软塑料管自制的氧气发生装置,无纺布包内药品为_____,药品加入完毕后,接下来的操作是_____,收集所需的氧气。对该装置的评价,你认为合理的是_____;
A 实验室中所用仪器、材料均易得到,可充分利用资源 B 可随时控制反应的发生和停止
(4)已知一氧化氮气体难溶于水,在空气中易与氧气发生反应,则收集一氧化氮气体时应选用图中的装置_____(填序号);
(5)用装置F收集氧气,验满时将带火星的木条放在_____(填“a”或“b”)处;
(6)将A、G装置相连收集氧气并测量氧气的体积,下列说法正确的是_____;
A 加热时间过短,会使测量结果不准;
B 反应一段时间后,排出反应装置内原有空气再连接G装置收集气体,会使结果更准确。
【答案】分液漏斗 水槽 没有对准药品集中的部位加热或药品不纯 没有等冒出连续均匀的气泡就开始收集或没等集气瓶口有气泡冒出,就将集气瓶从水槽中取出 可以控制反应速率 二氧化锰 挤压软塑料管中下部 AB E b A
【解析】
(1)由图可知,仪器①为分液漏斗,仪器②为水槽,故填写:分液漏斗、水槽;
(2)气密性良好,加热过程中E装置内导管口始终没有气泡冒出,其可能原因是没有对准药品集中的部位加热或药品不纯,故填写:没有对准药品集中的部位加热或药品不纯(任写一条);
制得的氧气不纯,可能的原因是没有等冒出连续均匀的气泡就开始收集或没等集气瓶口有气泡冒出,就将集气瓶从水槽中取出,故填写:没有等冒出连续均匀的气泡就开始收集或没等集气瓶口有气泡冒出,就将集气瓶从水槽中取出(任写一条);
(3) 装置B中有分液漏斗,它可以控制液体的滴加速率,从而控制反应速率,故填写:可以控制反应速率;
无纺布包内是固体药品,而固液制氧气的药品只有液体过氧化氢和固体二氧化锰,故填写:二氧化锰;
药品加入完毕后,接下来的操作是挤压软塑料管中下部,使液体与固体接触,发生反应,故填写:挤压软塑料管中下部;
装置H实验中所用仪器、材料均易得到,可充分利用资源,故符合题意,
可以通过挤压或放松软塑料管中下部,控制反应的发生和停止,故符合题意;
(4) 一氧化氮气体难溶于水,在空气中易与氧气发生反应,因此,不能用排空气法收集,只能用排水法收集,故填写:E;
(5)氧气验满时,将带火星的木条放在集气瓶口,观察木条是否复燃,故填写:b;
(6) 将A、G装置相连收集氧气并测量氧气的体积,若是加热时间过短,会使测量结果不准,正确;反应一段时间后,排出反应装置内原有空气再连接G装置收集气体,会导致一部分氧气进入空气中,不会使结果更准确,错误;
故填:A.

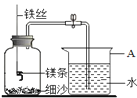
【题目】小婧同学学习化学后知道,镁在氧气中燃烧会生成白色的氧化镁固体.但她在空气中点燃镁条时,却发现在生成的白色固体中还夹杂着少量的淡黄色固体.
【提出问题】为什么会生成淡黄色固体?
【查阅资料】小婧查阅资料,记录了下列几种物质的颜色:
物 质 | MgO | MgCl2 | Mg3N2 | Mg(NO3)2 | MgCO3 | Mg(OH)2 |
颜 色 | 白色 | 白色 | 淡黄色 | 白色 | 白色 | 白色 |
其他同学认为不必查阅氯化镁的颜色,理由是 ;
【提出猜想】分析资料,小婧认为淡黄色固体可能是由镁与空气中的 反应生成的;
【实验探究】小婧设计实验证实了自己的猜想,她的方案可能 ;
【实验结论】根据小婧的实验结果,写出镁条在空气中燃烧时两个反应的化学方程式: 、
【反思与评价】通过上述实验,你对燃烧有什么新的认识? .