题目内容
【题目】实验室有瓶过了保质期的淡黄色固体药品,标签上名称为“过氧化钠(Na2O2)”。某研究小组在老师指导下对其成分和性质进行如下探究。
(查阅资料)I.过氧化钠是一种淡黄色固体,常用在呼吸面具和潜艇中产生氧气。其原理是:2Na2O2+2H2O=4NaOH+O2↑,2Na2O2+2CO2=2Na2CO3+O2
Ⅱ.常温、常压下O2的密度为1.3g/L。
(分析猜想)
(1)该小组同学认为,不做实验,就可以判断该物质中一定含Na2O2,理由是_____。
(2)进一步对固体成分提出以下猜想:I.只有Na2O2;Ⅱ.含有Na2O2、NaOH两种物质;Ⅲ.含有_____两种物质;Ⅳ.含有_____三种物质。
(实验探究)
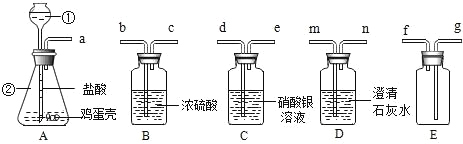
按如图的所示连接好装置。用电子天平秤取2.00g样品于干燥的装置中,分液漏斗中添加一定量的蒸馏水。
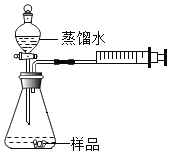
(3)打开分液漏斗活塞,将水滴加到锥形瓶中。反应完全后无固体剩余,注射器中收集到80mL气体,说明样品中含有_____gNa2O2(结果保留到小数点后两位,下同)。
(4)向反应后溶液中滴加酚酞,溶液显红色,说明反应后溶液显_____(选填“酸性”或“碱性”),小明认为原固样品体样品中一定含有氢氧化钠,你认为他的观点_____(选填“正确”或“不正确”),理由是_____。
(5)继续向锥形瓶中滴加足量的氯化钡溶液,有白色沉淀生成,静置,上层清液红色不褪,根据实验可以确定滴加酚酞溶液前锥形瓶中溶液含有的溶质是_____(填化学式)。
(6)将锥形瓶中混合物经过过滤、洗涤、干燥等,称得固体质量为1.97g。
(得出结论)
通过以上实验得出猜想_____成立。氢氧化钠的质量为_____g。
(反思与提高)
过氧化钠长期暴露在空气中,最终会变质为_____(填化学式)。
【答案】过氧化钠是淡黄色固体,而氢氧化钠和碳酸钠都是白色固体 Na2O2和Na2CO3 Na2O2、NaOH、Na2CO3 0.51 碱性 不正确 过氧化钠能与水反应生成氢氧化钠,碳酸钠溶液也显碱性 Na2CO3、NaOH Ⅳ 0.43 Na2CO3
【解析】
[分析猜想]
(1)不用做实验,仅由查得的资料和所学知识就可推断该固体一定含有Na2O2,理由是过氧化钠是淡黄色固体,而氢氧化钠和碳酸钠都是白色固体。故填:过氧化钠是淡黄色固体,而氢氧化钠和碳酸钠都是白色固体;
(2)因为:2Na2O2+2H2O=4NaOH+O2↑,2Na2O2+2CO2=2Na2CO3+O2,所以进一步对固体成分提出以下猜想:
Ⅰ.只有Na2O2;
Ⅱ.含有Na2O2、NaOH两种物质;
Ⅲ.含有Na2O2和Na2CO3两种物质;
Ⅳ.含有Na2O2、NaOH、Na2CO3三种物质。
故填:Na2O2和Na2CO3;Na2O2、NaOH、Na2CO3。
[实验探究]
(3)反应完全后(无固体剩余),注射器内收集到80.0mL气体,该气体是氧气,氧气质量为:1.3g/L×0.08L=0.104g,
设过氧化钠质量为x,
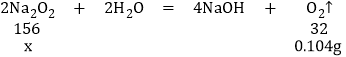
![]()
x≈0.51g
故填:0.51。
(4)向反应后溶液中滴加酚酞,溶液显红色,说明反应后溶液显碱性,碳酸钠溶液、氢氧化钠溶液均显碱性,过氧化钠也能与水反应生成氢氧化钠,所以小明的观点是错误的,故填:碱性;不正确;过氧化钠能与水反应生成氢氧化钠,碳酸钠溶液也显碱性;
(5)氯化钡与氢氧化钠不反应,但是能与碳酸钠反应生成碳酸钡白色沉淀,所以继续向锥形瓶中滴加足量的氯化钡溶液,有白色沉淀生成说明可以确定滴加酚酞溶液前锥形瓶中溶液含有碳酸钠,静置,上层清液红色不褪,说明可以确定滴加酚酞溶液前锥形瓶中溶液还含有氢氧化钠;故填:Na2CO3、NaOH;
(6)设碳酸钠的质量为y,则:
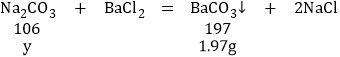
![]()
y=1.06g
[得出结论]由以上实验过程、实验现象可知,该固体中含有Na2O2、NaOH、Na2CO3三种物质,即猜想Ⅳ成立;
其中氢氧化钠的质量为:2.00g﹣0.51g﹣1.06g=0.43g;故填:Ⅳ;0.43;
[反思与提高]过氧化钠暴露在空气中,与空气中二氧化碳反应生成碳酸钠和氧气,与空气中的水蒸气反应生成氢氧化钠和氧气,氢氧化钠与二氧化碳反应合成碳酸钠,所以过氧化钠长期暴露在空气中,最终会变质为碳酸钠;故填:Na2CO3。