题目内容
【题目】通过对化学的学习,你已掌握了实验室制取气体的有关规律,请结合下图回答有关问题: 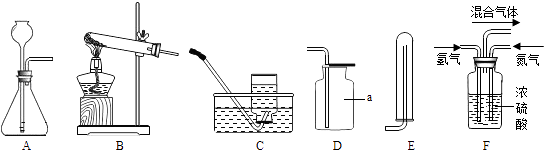
(1)图中标有a的仪器名称是 .
(2)实验室用氯酸钾制取氧气,反应的化学方程式为 , 可选择的收集装置是D或(填字母,下同).
(3)实验室用锌和稀硫酸制取氢气,应选择的发生装置是 , 反应的化学方程式为 .
(4)氨气是一种无色、有刺激性气味、极易溶于水的气体,可用于制氮肥、硝酸、药物和燃料等. ①实验室用加热氯化铵和熟石灰的固体混合物的方法制取氨气,则实验室制取并收集氨气应选择的装置组合是 .
②工业上用氮气和氢气合成氨气(反应的化学方程式:N2+3H2 ![]() 2NH3).
2NH3).
实验室模拟合成氨气的流程如下: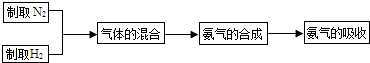
流程中“气体的混合”是在F装置中进行的,F装置的作用有三个:一是将氮气和氢气干燥;二是使氮气和氢气充分混合;三是 , 从而提高氮气和氢气的利用率.
【答案】
(1)集气瓶
(2)2KClO3 ![]() 2KCl+3O2↑;C
2KCl+3O2↑;C
(3)A;Zn+H2SO4═ZnSO4+H2↑
(4)BE;使氢气和氮气气流稳定
【解析】解:(1)图中a是集气瓶.所以答案是:集气瓶.(2)实验室用氯酸钾制取氧气,反应的化学方程式为2KClO3 ![]() 2KCl+3O2↑.氧气的密度大于空气的密度,并且不易溶于水,所以用装置C或D收集.所以答案是:2KClO3
2KCl+3O2↑.氧气的密度大于空气的密度,并且不易溶于水,所以用装置C或D收集.所以答案是:2KClO3 ![]() 2KCl+3O2↑;C.(3)①根据信息:氨气是一种无色、有刺激性气味、极易溶于水的气体,和用加热氯化铵和熟石灰的固体混合物的方法制取氨气.可知是固体的加热反应,所以用装置B作发生装置;氨气的密度小于空气的密度,极易溶于水,所以收集装置用E.所以答案是:BE;②F装置的作用有三个:一是将氮气和氢气干燥;二是使氮气和氢气充分混合;三是通过观察F中的气泡控制氮气和氢气的流量,使氢气和氮气气流稳定,达到最佳比例.所以答案是:使氢气和氮气气流稳定.
2KCl+3O2↑;C.(3)①根据信息:氨气是一种无色、有刺激性气味、极易溶于水的气体,和用加热氯化铵和熟石灰的固体混合物的方法制取氨气.可知是固体的加热反应,所以用装置B作发生装置;氨气的密度小于空气的密度,极易溶于水,所以收集装置用E.所以答案是:BE;②F装置的作用有三个:一是将氮气和氢气干燥;二是使氮气和氢气充分混合;三是通过观察F中的气泡控制氮气和氢气的流量,使氢气和氮气气流稳定,达到最佳比例.所以答案是:使氢气和氮气气流稳定.
【考点精析】本题主要考查了氢气的制取和检验和书写化学方程式、文字表达式、电离方程式的相关知识点,需要掌握氢气的实验室制法原理:Zn + H2SO4 = ZnSO4 +H2↑;Zn + 2HCl = ZnCl2 +H2↑不可用浓盐酸的原因 浓盐酸有强挥发性 ;不可用浓硫酸或硝酸的原因 浓硫酸和硝酸有强氧化性;注意:a、配平 b、条件 c、箭号才能正确解答此题.

 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案【题目】碘酸钾(KIO3)主要用作食盐加碘剂 Ⅰ、制备碘酸钾
实验室制备碘酸钾的路线如下:
干海带→I2 ![]() HIO3
HIO3 ![]() KIO3
KIO3
(1)KIO3中I的化合价为 , 含碘盐中的碘是指(填字母). a、离子 b、元素 c、分子
(2)实验中需要用试纸测定溶液的pH,其操作方法是 .
(3)过滤操作需要的玻璃仪器有玻璃棒、烧杯和 .
(4)用冰水洗涤过滤所得KIO3晶体,其原因是 .
(5)温度过高,会造成H2O2利用率降低,可能的原因是 .
(6)Ⅱ测定碘含量 资料:
①碘酸钾与碘化钾反应方程式为:KIO3+5KI+3H2SO4═3K2SO4+3H2O+3I2
②淀粉溶液遇碘显色时,碘浓度越大颜色越深;
③扬州作为轻度缺碘地区,食盐中碘含量(以I计)应为18~33mg/Kg
步骤1:配置以下各种试剂:100g/L食盐溶液,2.14×10﹣3g/L KIO3溶液,测试液(含10g/L淀粉、196g/L H2SO4、1.66g/L KI).
步骤2:取5支相同规格小试管,贴上编号标签,按下表要求分别依次加入步骤1中配置的KIO3溶液,测试液、蒸馏水,塞上橡皮塞,混合后有序放置在试管架上(各试管中KIO3完全反应).
试管编号 | 1 | 2 | 3 | 4 | 5 |
KIO3溶液滴数 | 30 | 25 | 20 | 15 | 10 |
测试液滴数 | 10 | 10 | 10 | 10 | 10 |
蒸馏水滴数 | 0 | 5 | 10 | 15 | 20 |
步骤3:另取一支小试管,一次加入步骤1中所配置的食盐溶液10滴、测试液10滴、和蒸馏水20滴,混合后与步骤2中各试管内颜色对照.
步骤3所得溶液呈色,则说明该食盐是含碘盐.
(7)步骤2实验的目的是 , 步骤2中测试液的滴数保持一致的原因是 .
(8)若步骤3所得溶液颜色与3号试管一致,则100mL该食盐溶液中含有碘酸钾mg.该食盐中碘含量为mg/Kg,扬州地区要求(填“符合”或“不符合”).