题目内容
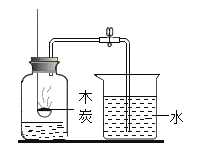
【题目】化学兴趣小组为验证质量守恒定律,按照如图装置进行实验,称取24g镁粉在空气中燃烧,发现产物中有少量黄色固体。
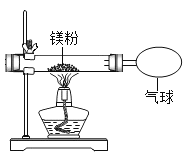
(提出问题)黄色固体是什么呢?
(查阅资料)
①氧化镁为白色固体;
②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水剧烈反应产生
氨气,该气体能使湿润的红色石蕊试纸变蓝
(做出猜想)黄色固体是Mg3N2.
(实验探究)请设计实验,验证猜想。
实验操作 | 实验现象及结论 |
取燃烧后的产物于试管中,加少量_____,再将_____放在试管口,观察观象。 | 观察到_____,说明燃烧产物中含有Mg3N2。 |
(反思与交流)(1)Mg3N2中氮元素的化合价为_____。
(2)空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的 MgO却远多于Mg3N2,其原因是_____。
(3)写出镁条在氮气中燃烧的化学方程式:_____。
【答案】水 湿润的红色石蕊试纸 有刺激性气味的气体生成,试纸由红色变为蓝色 -3 氮气化学性质不如氧气活泼 3Mg+N2![]() Mg3N2
Mg3N2
【解析】
[实验探究]需要验证氮化镁就要了解它的性质,氮化镁可与水剧烈反应产生氨气;而氨气有刺激性气味,能使湿润的红色石蕊试纸变蓝;所以设计的实验操作是取产物中的黄色固体放入试管中,加入适量的水,并在试管口放置湿润的红色石蕊试纸,实验现象是有刺激性气味的气体生成,试纸由红色变为蓝色;
[反思与交流](1)根据在化合物中正负化合价代数和为零,则氮化镁中氮元素的化合价为:(+2)×3+x×2=0,则x=-3;
(2)由于氮气的化学性质没有氧气活泼,因此,尽管空气中N2的含量远大于O2的含量,但是镁条在空气中燃烧产物MgO却远多于Mg3N2;
(3)镁条和氮气在点燃条件下生成氮化镁,反应的化学方程式:3Mg+N2![]() Mg3N2。
Mg3N2。

【题目】碳和碳组成的化合物是初中化学研究的重要内容,请认真阅读题目,完成下列问题。
(1)现代生活倡导“低碳生活”,主要是为了减少_______(填化学式)的排放量。
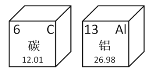
(2)组成化合物种类最多的元素是碳,如图所示,是元素周期表的一格。下列说法不正确的是__________。

A碳属于非金属元素 B碳元素的相对原子质量为12.01g
C碳原子中含有6个中子 D碳元素位于元素周期表的第ⅥA族
(3)吹不灭的蜡烛实验中,蜡烛中混有镁粉。已知镁条在二氧化碳气体中燃烧生成碳和氧化镁,请书写其化学方程式为__________;根据上述内容,你对燃烧知识有何新认识_________。
(4)如图是初中化学中常见仪器装置,回答下列问题:

①用大理石和稀盐酸制取并收集二氧化碳,可选用的装置是________,为防止气体从发生装置泄漏的必要措施是___________。
②F装置有多种用途。除去一氧化碳中的二氧化碳时,瓶中液体可以是_________。
A浓硫酸 B烧碱溶液 C浓盐酸 D饱和的碳酸氢钠溶液
(5)石灰厂为了测定一批石灰石样品中碳酸钙的质量分数,取用45g石灰石样品,把200g稀盐酸分四次加入样品中(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶于水),充分反应后过滤、干燥等操作,最后称量,得实验数据如下表:
稀盐酸的用量 | 第一次加入50g | 第二次加入50g | 第三次加入50g | 第四次加入50g |
剩余固体的质量 | 35g | 25g | 15g | 9g |
请计算该盐酸的溶质质量分数________。