题目内容
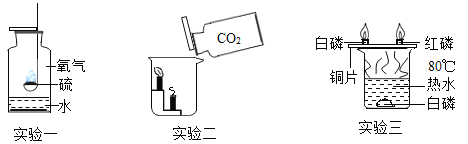
【题目】某化学实验小组利用以下装置测定某赤铁矿中氧化铁的纯度:
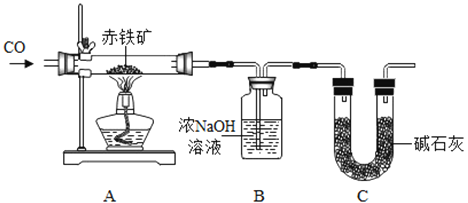
向赤铁矿中通人纯净的一氧化碳气体,假设赤铁矿中杂质不参与反应,请回答下列问题:
(1)实验开始时,先进行的操作是_____________(填序号)。
①通入一氧化碳 ②加热
(2)实验过程中观察到装置A中玻璃管内发生的现象______________。
(3)B装置发生的化学反应方程式是_______________;装置C的作用是________________。
(4)从环境保护的角度看该实验存在的缺陷是_______________。
(5)实验前称量赤铁矿的质量为20g。通入足量的一氧化碳完全反应后B装置总质量增加了13.2g,则赤铁矿中氧化铁的质量分数是多少?写出计算过程____________。
【答案】① 红色粉末逐渐变黑 2NaOH+CO2=Na2CO3+H2O 防止空气进入B装置 结尾处点燃或收集气体 80%
【解析】
(1)该实验中为了防止爆炸,要先通入一段时间的一氧化碳,排尽管中的空气,故选①。
(2)装置A中观察的现象是红色粉末逐渐变黑。
(3)B装置中是二氧化碳与氢氧化钠反应,生成碳酸钠和水,反应的方程式为:2NaOH+CO2=Na2CO3+H2O。装置C的作用是防止空气进入B装置,使测得的二氧化碳的质量不准确。
(4)该实验中有有毒气体一氧化碳,故为了防止污染空气,需要在装置结尾处点燃或收集气体。
(5)由题干可知,生成二氧化碳的质量为13.2g
设20g样品中氧化铁的质量为x

解得x=16g
赤铁矿中氧化铁的质量分数为:![]() ×100%=80%。
×100%=80%。

【题目】有A、B、C三种元素,它们形成的粒子结构示意图如下,其中说法正确的是( )
元素 | A | B | C |
其形成的粒子结构示意图 |
|
|
|
A. 它们之间可形成化学式为AC的化合物
B. 它们原子的核外电子层数相同
C. A的粒子结构示意图表示的是原子, B、C表示的是阳离子
D. 它们之间可形成化学式为B2A的化合物
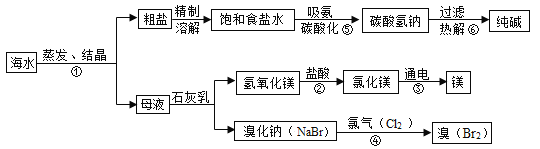
【题目】海水是巨大的资源宝库,如下图所示利用海水为原料可获得许多化工产品,下表为部分物质的溶解度,回答下列问题。
温度/℃ | 0 | 10 | 20 | 30 | 40 |
溶解度/g | NaCl | 35.8 | 36.0 | 36.3 | 36.6 |
NaHCO3 | 8.2 | 9.6 | 11.1 | 12.70 | |
NH4Cl | 33.2 | 37.21 | 41.4 | 45.8 |
(1)步骤①中选用蒸发结晶法而不用降温结晶法的理由是____________。
(2)步骤②发生反应的化学方程式是________,其基本反应类型为____________;步骤③中是电能转化为__________能。
(3)步骤④是向溴化钠中通入氯气,生成溴单质和一种盐,发生的是置换反应,试写出该反应的化学方程式______________。
(4)步骤⑤中碳酸氢钠先结晶析出,原因是____________;进行生产时,先向饱和食盐水中通入氨气,再加压不断通人二氧化碳气体,其理由是____________。
(5)写出步骤⑥的化学方程式__________________。