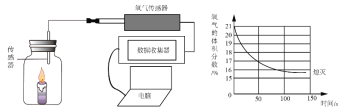
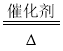题目内容
【题目】(1)化学用语是最简明、信息丰富、国际通用的语言,请用化学用语填空:
①2个氢原子:___________。
②二氧化氮分子:_________。
③硝酸根离子:__________。
④氧化铁中铁元素的化合价:____________。
(2)写出符号“2NH3”中数字的含义:“2”表示:__________“3”表示_____________。
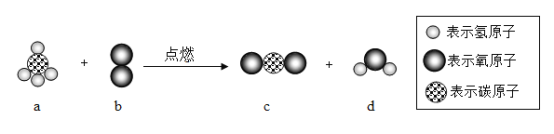
【答案】2H NO2 NO3- ![]() 两个氨分子 每一个氨分子中含有三个氢原子
两个氨分子 每一个氨分子中含有三个氢原子
【解析】
(1)①原子符号前面的数字表示原子个数,2个氢原子:2H;
②分子符号前面的数字表示分子个数。二氧化氮分子:2NO2;
③硝酸根离子带一个单位负电荷:NO3-;
④氧化铁中氧元素为-2价,铁元素为+3价:![]() ;
;
(2)符号“2NH3”中:分子符号前面的数字表示分子个数“2”表示:2个氨分子;元素符号右下角的数字表示原子个数,“3”表示:每一个氨分子中含有三个氢原子;

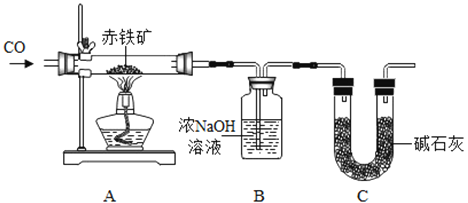
【题目】如图所示,把足量的硫粉放入氧气中充分燃烧。
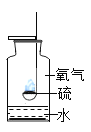
(1)硫在氧气中燃烧的化学方程式是___________________________。
(2)实验后,取少量集气瓶内的溶液于试管中,再往试管中滴加数滴的紫色石蕊溶液,振荡。发现紫色石蕊溶液变成红色。(提示:石蕊溶液是将石蕊加入水中溶解后得到的混合物)
[提出问题]是什么物质使紫色石蕊变红色呢?
[提出假设]假设1:水使紫色石蕊变红;
假设2:__________________使紫色石蕊变红;
假设3:二氧化硫与水反应的生成物使紫色石蕊变红。
[设计实验]
①我们可判断假设________________不成立,因为石蕊溶液中含有这种物质,不能使紫色变红。
②请设计一个实验方案验证另外两个假设是否成立,用文字描述实验步骤及填写预期实验现象和结论。(提供的试剂和用品有:干燥的紫色石蕊纸花若干朵、干燥的二氧化硫两瓶、水)
实验步骤 | 预期实验现象和结论 |
将干燥的紫色石蕊纸花,放入盛有______________瓶中。 | _________________,假设2不成立。 |
将干燥的紫色石蕊纸花_______________后放入盛有干燥的二氧化硫的瓶中。 | ________________________,假设______________成立。 |
【题目】学习金属的化学性质时,老师给同学们做了锌与稀硫酸反应制取氢气的实验。有同学问老师:可以用锌与浓硫酸反应来制取氢气吗?老师让同学们先去查资料,然后对锌与浓硫酸反应产生的气体进行探究
(提出问题)锌与浓硫酸完全反应产生的气体是什么?
(查阅资料)
(1)浓硫酸是强氧化性酸,能与多数金属(如Mg、Zn、Cu等)反应产生SO2。
锌与浓硫酸反应:![]()
(2)SO2是一种有刺激性气味的有毒气体,与CO2有相似的化学性质,与Ca(OH)2反应产生不溶于水的CaSO3(提出猜想)猜想1:只有SO2 猜想2:H2和SO2 猜想3:_____。
(实验探究)
同学们在老师指导下设计并进行如下图的实验:
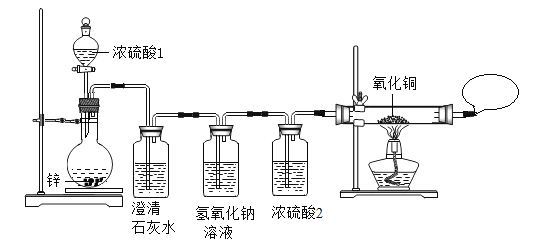
(现象与结论)
实验现象 | 实验结论 |
(1)_____。 | 有SO2产生。 |
(2)黑色的氧化铜变红色 | _____。 |
(得出结论)猜想_____正确。
(反思与拓展)
(1)实验中两处用了浓硫酸。浓硫酸2的作用是_____。
(2)有同学提出:实验进行到后阶段才能观察到黑色的氧化铜逐渐变红色。请解释实验开始阶段CuO处没有明显现象的原因:_____。
(3)实验室用金属与浓硫酸反应制取较纯的SO2气体,现有金属Zn和Cu最好选用金属_____理由是_____。
【题目】在一个密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表.则关于此反应的说法正确的是( )
物 质 | X | Y | Z | W |
反应前的质量(g) | 2 | 1 | 16 | 16 |
反应后的质量(g) | 12 | m | 8 | 14 |
A.物质Y一定是该反应的催化剂
B.该反应的基本类型为分解反应
C.参加反应的Z与W的质量比为4:1
D.反应后生成X的质量为12 g
【题目】现有25 g石灰石样品,请按下面要求计算:
(1)25 g样品与足量的稀盐酸反应放出8.8 gCO2(杂质不溶于酸,且不与酸反应),请计算该样品的纯度(CaCO3的质量分数)是多少_______?
(2)若将25 g样品平均分成两份,分别加工成块状和粉末状,将两份样品分别放入锥形瓶中,同时加入相同体积,相同浓度的足量稀盐酸充分反应,请在图像上画出块状样品和粉末状药品与稀盐酸反应放出CO2的曲线示意图______。
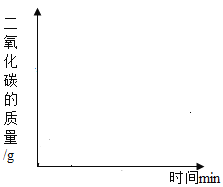
(3)若将一定质量的该石灰石样品高温煅烧,有关物质质量随反应时间的变化如表所示:
时间/min | t1 | t2 | t3 | t4 | t5 |
CO2质量/g | 2.2 | 4.4 | 6.6 | 8.8 | 8.8 |
剩余固体质量/g | 22.8 | 20.6 | m | 16.2 | 16.2 |
则m=_______,t3时剩余固体中除杂质外含有的物质是_____(填化学式)。