题目内容
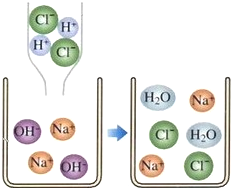
【题目】将高锰酸钾溶液和双氧水混合,得到KOH溶液并出现如下图所示现象.
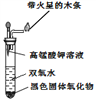
(1)双氧水中氧元素的化合价为________.
(2)反应的化学方程式是________ .
【答案】 -1 2KMnO4+H2O2=2MnO2+2KOH+2O2↑或2KMnO4+3H2O2=2MnO2+2KOH+3O2↑+2H2O
【解析】(1)双氧水中氢元素为+1价,设氧元素的化合价为x ,根据化合物中化合价的代数和为零,+1![]() 2+2x=0,x=-1,所以双氧水中氧元素的化合价为-1价;(2)高锰酸钾和双氧水反应生成二氧化锰、氢氧化钾和氧气(或高锰酸钾和双氧水反应生成二氧化锰、氢氧化钾、氧气和水),反应的化学方程式是:2KMnO4+H2O2=2MnO2+2KOH+2O2↑或2KMnO4+3H2O2=2MnO2+2KOH+3O2↑+2H2O。
2+2x=0,x=-1,所以双氧水中氧元素的化合价为-1价;(2)高锰酸钾和双氧水反应生成二氧化锰、氢氧化钾和氧气(或高锰酸钾和双氧水反应生成二氧化锰、氢氧化钾、氧气和水),反应的化学方程式是:2KMnO4+H2O2=2MnO2+2KOH+2O2↑或2KMnO4+3H2O2=2MnO2+2KOH+3O2↑+2H2O。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】向100g水中不断加入固体A或改变温度,得到相应的溶液①~⑤。下列说法正确的是( )
![]()
资料:A的溶解度 | |||||
温度/℃ | 20 | 30 | 40 | 50 | 60 |
溶解度/g | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 |
A. ②中A的质量分数最大 B. ③⑤中A的质量分数相等
C. ②④⑤的溶液为饱和溶液 D. ①③④⑤中没有固体存在