��Ŀ����
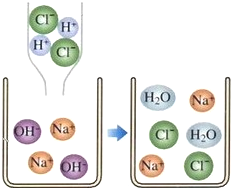
����Ŀ�����л�ѧ�У�����ѧϰ����ͼ���кͷ�Ӧ��ʵ����H++OH��=H2O��������ʵ�ʲμӷ�Ӧ�����ӷ�������ʾ��Ӧ��ʽ�ӽ����ӷ���ʽ�����ӷ���ʽ����дһ�㰴���²��裺(��Na2SO4��BaCl2��ӦΪ��)��д��Na2SO4��BaCl2��Ӧ�Ļ�ѧ����ʽ��___________�� �ڰ�������ˮ������д��������ʽ�������ܵ����ʡ������ˮ�����û�ѧʽ��ʾ����������ʽ�ɸ�д�ɣ�2Na��+SO42-+Ba++2Cl-=BaSO4��+2Na��+2Cl- ��ɾȥ����ʽ���߲��μӷ�Ӧ�����ӣ�Ba2++SO4-�TBaSO4���� �ܼ�鷽��ʽ���߸�Ԫ�ص�ԭ�Ӹ����͵�������Ƿ���ȡ�
��ش�
(1)���и����е����ӣ�������Һ�д����������________
A��Na+��Mg2+��Cl����SO4 �� B��Na+��H+��Cl����OH��
C��Na+��Cu+��Cl����SO42�� D��Na+��NH4+��Cl����OH��
(2)д��ϡ�������ʯ��ʯ����������Ӧ�����ӷ���ʽ_________.
(3)д��һ�������ӷ���ʽMg+2H+=Mg2++H2�����Ӧ�Ļ�ѧ����ʽ________��
���𰸡� Na2SO4+BaCl2=BaSO4��+2NaCl AC CaCO3+2H+=Ca2++H2O+CO2�� Mg+H2SO4=MgSO4+H2����Mg+2HCl=MgCl2+H2��
�����������⿼���˸��ֽⷴӦ���������ֽⷴӦ��ʵ�ʡ�
��Na2SO4��BaCl2�������ֽⷴӦ������ɷ�����BaSO4��NaCl����Ӧ�Ļ�ѧ����ʽ�ǣ�Na2SO4+BaCl2=BaSO4��+2NaCl
��1��A���������Ӽ䲻�ܽ�ϳɳ����������ˮ���ܴ������棬��ȷ��B��H+�� OH���������ˮ�����ܴ������棬����C���������Ӽ䲻�ܽ�ϳɳ����������ˮ���ܴ������棬��ȷ��D��NH4+����OH��������ɰ�����ˮ�����ܹ��棬����ѡAC��
��2��ϡ�������ʯ��ʯ����������Ӧ�����ӷ���ʽ�ǣ�CO32��+2H+=H2O+CO2��
��3�������ӷ���ʽMg+2H+=Mg2++H2�����Ӧ�Ļ�ѧ����ʽ����Ϊ��Mg+H2SO4=MgSO4+H2����Mg+2HCl=MgCl2+H2����

 �Ͻ�ƽСѧ��������ϵ�д�
�Ͻ�ƽСѧ��������ϵ�д� �Ƹ������������ϵ�д�
�Ƹ������������ϵ�д�