题目内容
【题目】人类文明与社会进步同金属材料密切相关。
(1)2018年12月29日,南京长江大桥恢复通车。为保证大桥的使用寿命,下列防锈措 施可行的是___。
A.用抗腐蚀性能优异的合金制造造桥零部件B.刷防锈漆
C.桥身表面镀一层黄金D.给某些部位涂油
(2)造桥需要钢铁,工业炼铁的原料有铁矿石、石灰石、___和热空气;钢铁材料分为生铁和钢,这两种铁合金的主要区别就在于___。
(3)将光亮镁条放入一定量的氯化铵溶液中,发现最终生成灰白色固体[Mgx(OH)yClz]外, 还有气体生成。某同学对该现象作如下探究。
(一)生成气体可能是 H2、HCl、NH3 中的一种或几种。
(查阅资料)
①浓硫酸既可以吸收水,也可吸收氨气;
②常温下,氨气和氯化氢气体反应生成白色固体氯化铵(NH4Cl);
③2NH3+3CuO![]() 3Cu+N2+3H2O;
3Cu+N2+3H2O;
④H2+CuO![]() Cu+H2O。
Cu+H2O。
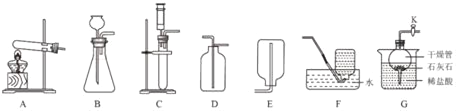
(实验探究)收集气体,将气体通过如图装置(各步反应均完全);
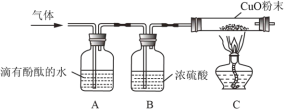
①A装置中出现红色,证明有___;
②A、B 实验装置___(填“能”或“不能”)对调,理由是___;
③C 中玻璃管内观察到___,证明有H2。
(反思与评价)他认为不需要单独检验HCl,就能证明HCl不存在,请你评价这种说法是 否合理并说明理由___。
(二)过滤、洗涤、一定温度下烘干得灰白色固体。
(查阅资料)灰白色固体Mgx(OH)yClz 受热会分解,只生成MgO和HCl。
(实验探究)
取一定量灰白色固体样品,充分加热,得到4g白色固体和3.65g气体。
(结论)
①x : z=___;
②若所得灰白色固体的相对分子质量为153,则所得灰白色固体的化学式是___。
(反思与评价)
由同学认为,不属于任何数据,就可以求出x:z的值,请你说出理由___
【答案】ABD; 焦炭 含碳量不同 NH3 不能 浓硫酸会吸收氨气,无法检验氨气的存在 黑色固体变成红色 合理,NH3能和HCl反应生成NH4Cl,NH3一定存在,则HCl一定不存在 1:1 Mg2(OH)2Cl2 Mgx(OH)yClz 受热分解,只生成 MgO 和 HCl,根据化学式可知氢氧原子个数 比为 1:1,则生成 MgO 和 HCl 的分子个数比为 1:1,其中 Mg、Cl 原子个数比,即 x:z 为 1:1。
【解析】
(1)A、用抗腐蚀性能优异的合金制造造桥零部件,能防止零部件生锈,故A正确;
B、刷防锈漆,能隔绝氧气和水,能防止零部件生锈,故B正确;
C、桥身表面镀一层黄金,黄金资源有限、价格太高等,是不现实的,故C错误;
D、给某些部位涂油,能隔绝氧气和水,能防止零部件生锈。故选ABD。
(2)工业上,高炉炼铁的原料除了铁矿石、空气、石灰石还需要焦炭,焦炭能提供热量,产生还原剂一氧化碳;钢铁材料分为生铁和钢,生铁的含碳量为2%~4.3%,钢的含碳量为0.03%~2%,这两种铁合金的主要区别在于含碳量不同;
(3)(一)实验探究:
①A装置中出现红色,说明氨气和水反应生成了氨水,氨水显碱性,能使酚酞试液变红色,因此可以证明有氨气(NH3);
②A、B实验装置不能对调,理由是浓硫酸能够吸收氨气,浓硫酸吸收氨气后,再进入酚酞试液中时,不能检验出氨气;
③氢气与氧化铜加热时生成铜和水。C中玻璃管内观察到黑色粉末变成红色,玻璃管内壁出现水珠,证明有H2;
反思与评价:
不需要单独检验HCl,就能证明HCl不存在,这种说法是合理,理由是NH3 能和 HCl 反应生成 NH4Cl,NH3一定存在,则HCl一定不存在;
(二)结论:
根据“灰白色固体Mgx(OH)yClz受热会分解,只生成MgO和HCl”和“取一定量灰白色固体样品,充分加热,得到4g白色固体和3.65g 气体”可知,灰白色固体样品质量为:4g+3.65g=7.65g,氧化镁的质量为4g,HCl气体为3.65g,所以其中镁元素质量=![]() ,氧元素质量为:4g﹣2.4g=1.6g,氢元素质量=
,氧元素质量为:4g﹣2.4g=1.6g,氢元素质量=![]() ,氯元素质量为:3.65g﹣0.1g=3.55g;根据灰白色固体[Mgx(OH)yClz]化学式有:24x:17y=2.4g:(1.6g+0.1g),24x:35.5z=2.4g:3.55g,解得:x:y:z=1:1:1,即该灰白色固体的化学式为Mgn(OH)nCln,若所得灰白色固体的相对分子质量为153,则:24n+17n+35.5n=153,n=2,所以其化学式为:Mg2(OH)2Cl2;
,氯元素质量为:3.65g﹣0.1g=3.55g;根据灰白色固体[Mgx(OH)yClz]化学式有:24x:17y=2.4g:(1.6g+0.1g),24x:35.5z=2.4g:3.55g,解得:x:y:z=1:1:1,即该灰白色固体的化学式为Mgn(OH)nCln,若所得灰白色固体的相对分子质量为153,则:24n+17n+35.5n=153,n=2,所以其化学式为:Mg2(OH)2Cl2;
反思与评价:由于Mgx(OH)yClz受热分解,只生成MgO和HCl,根据化学式可知氢、氧原子个数比为1:1,则生成MgO和HCl的分子个数比为1:1,其中Mg、Cl原子个数比,即x:z为1:1。

 阅读快车系列答案
阅读快车系列答案