题目内容
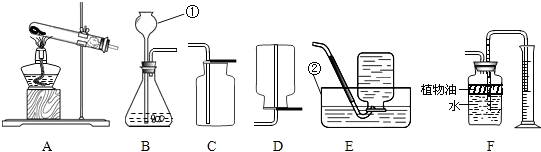
 如图所示装置可用来测定空气中氧气的含量.对该实验的认识不正确的是
如图所示装置可用来测定空气中氧气的含量.对该实验的认识不正确的是
- A.将红磷改为蜡烛也能得到正确的实验结论
- B.红磷的量不足会影响实验结论
- C.钟罩内气体压强的减小导致水面的上升
- D.装置应保证气密性良好
A
分析:本题是用红磷测定空气中氧气的含量,本探究实验一般要注意以下几点:①装置的气密性好;②所用药品红磷的量,必须是足量;③读数时一定要冷却到原温度;④生成物的状态一般要求是固态等.如果控制不好条件,进入集气瓶中水体积会小于五分之一.如果装置内的部分空气逸散出来,就会导致进入集气瓶中水体积大于五分之一.
解答:A、蜡烛燃烧生成二氧化碳气体,影响实验结果,符合题意,故选项正确;
B、所用药品红磷的量,必须是足量,正确但不符合题意,故选项错误;
C、反应后生成五氧化二磷固体,内外产生压强差,正确但不符合题意,故选项错误;
D、装置的气密性好,正确但不符合题意,故选项错误;
故选A.
点评:本考点是测定氧气在空气中的体积分数,这类探究实验中要注意以下几点:①装置的严密性②所用药品的量③生成物的状态④读数时要冷却到原温度等.要具体问题具体分析,根据设计的步骤中不同的现象去思考,从而得出正确的结论.本考点经常出现在选择题、填空题和实验题中.
分析:本题是用红磷测定空气中氧气的含量,本探究实验一般要注意以下几点:①装置的气密性好;②所用药品红磷的量,必须是足量;③读数时一定要冷却到原温度;④生成物的状态一般要求是固态等.如果控制不好条件,进入集气瓶中水体积会小于五分之一.如果装置内的部分空气逸散出来,就会导致进入集气瓶中水体积大于五分之一.
解答:A、蜡烛燃烧生成二氧化碳气体,影响实验结果,符合题意,故选项正确;
B、所用药品红磷的量,必须是足量,正确但不符合题意,故选项错误;
C、反应后生成五氧化二磷固体,内外产生压强差,正确但不符合题意,故选项错误;
D、装置的气密性好,正确但不符合题意,故选项错误;
故选A.
点评:本考点是测定氧气在空气中的体积分数,这类探究实验中要注意以下几点:①装置的严密性②所用药品的量③生成物的状态④读数时要冷却到原温度等.要具体问题具体分析,根据设计的步骤中不同的现象去思考,从而得出正确的结论.本考点经常出现在选择题、填空题和实验题中.

练习册系列答案
相关题目

 20、某课外活动小组研究外界条件对水中氧气含量的影响.他们利用仪器测得以下数据.
20、某课外活动小组研究外界条件对水中氧气含量的影响.他们利用仪器测得以下数据.