题目内容
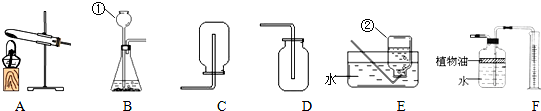
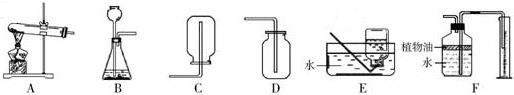
如图所示为实验室常用的实验装置:
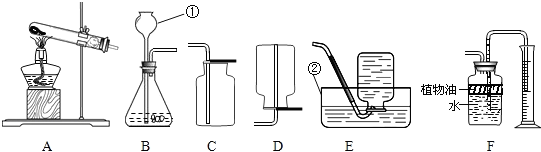
据图回答下列问题:
(1)写出带有标号的仪器名称:①
(2)实验室通常用石灰石与稀盐酸反应制取二氧化碳,应选用的发生装置是
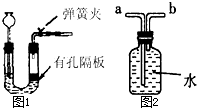
(3)F装置可用来测量生成的二氧化碳气体的体积,其中在水面上防一层植物油的目的是
(4)实验室用高锰酸钾(KMnO4)制取氧气,应选用的发生装置是
(5)某同学称取一定质量KMnO4放在大试管中,将温度控制在250℃加热制取O2,实验结束时,该同学发现收集到的O2大于理论产量,针对这一现象,同学们进行了如下探究:
【提出猜想】猜想l:反应生成的MnO2分解放出O2;猜想Ⅱ:反应生成的锰酸钾(K2MnO4)分解放出O2
做出上述猜想的理由是
【实验验证】同学们分为两组,分别进行以下实验:
①第一组同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变.则猜想
②第二组同学取K2MnO4在250℃条件下加热,没有用测定质量的方法,也得出了猜想Ⅱ正确的结论.该组同学选择的实验方法是
【拓展延伸】实验发现,K2MnO4受热只能部分分解,经分析可能是生成物氧化钾(K2O)对其分解产生影响.请设计实验方案验证:
【实验反思】通过以上实验探究,该生对“问题的发现与解决”有何认识:必须通过认真分析,用实验来加以证明.

据图回答下列问题:
(1)写出带有标号的仪器名称:①
长颈漏斗
长颈漏斗
,②水槽
水槽
.(2)实验室通常用石灰石与稀盐酸反应制取二氧化碳,应选用的发生装置是
B
B
(填序号,下同),收集装置是C
C
.该反应的文字表达式为碳酸钙+盐酸→氯化钙+二氧化碳+水
碳酸钙+盐酸→氯化钙+二氧化碳+水
.(3)F装置可用来测量生成的二氧化碳气体的体积,其中在水面上防一层植物油的目的是
防止二氧化碳溶于水,与水反应
防止二氧化碳溶于水,与水反应
,植物油上方原有的空气对实验的结果没有
没有
(填“有”或“没有”) 明显影响.(4)实验室用高锰酸钾(KMnO4)制取氧气,应选用的发生装置是
A
A
,收集装置是C或E
C或E
.该反应的文字表达式为高锰酸钾
锰酸钾+二氧化锰+氧气
| 加热 |
高锰酸钾
锰酸钾+二氧化锰+氧气
.该反应属于| 加热 |
分解反应
分解反应
基本反应类型.(5)某同学称取一定质量KMnO4放在大试管中,将温度控制在250℃加热制取O2,实验结束时,该同学发现收集到的O2大于理论产量,针对这一现象,同学们进行了如下探究:
【提出猜想】猜想l:反应生成的MnO2分解放出O2;猜想Ⅱ:反应生成的锰酸钾(K2MnO4)分解放出O2
做出上述猜想的理由是
它们都是含有氧元素的化合物
它们都是含有氧元素的化合物
.【实验验证】同学们分为两组,分别进行以下实验:
①第一组同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变.则猜想
1
1
错误.②第二组同学取K2MnO4在250℃条件下加热,没有用测定质量的方法,也得出了猜想Ⅱ正确的结论.该组同学选择的实验方法是
制得了一些氧气
制得了一些氧气
.【拓展延伸】实验发现,K2MnO4受热只能部分分解,经分析可能是生成物氧化钾(K2O)对其分解产生影响.请设计实验方案验证:
取等量的锰酸钾固体于两支试管中,一支试管中加入氧化钾,一支试管中不加入氧化钾.用同样火焰的酒精灯加热,用相同规格的集气瓶,用排水法收集一瓶气体,收集一瓶氧气所用的时间作比较,确定锰酸钾的分解是否与氧化钾有关系.
取等量的锰酸钾固体于两支试管中,一支试管中加入氧化钾,一支试管中不加入氧化钾.用同样火焰的酒精灯加热,用相同规格的集气瓶,用排水法收集一瓶气体,收集一瓶氧气所用的时间作比较,确定锰酸钾的分解是否与氧化钾有关系.
.【实验反思】通过以上实验探究,该生对“问题的发现与解决”有何认识:必须通过认真分析,用实验来加以证明.
分析:(1)根据制取气体的反应原理来解答该题.
(2)根据装置的适用范围来选择合适结合反应原理来选择发生装置,根据收集气体时所选的装置的适用范围来判断气体的性质.
(2)根据装置的适用范围来选择合适结合反应原理来选择发生装置,根据收集气体时所选的装置的适用范围来判断气体的性质.
解答:解:AB应属于发生装置,其余的是收集装置.装置A适于固体加热的反应,而装置B适于固液不需要加热的反应,c适于密度大于空气的气体收集装置,D适于密度小于空气的气体收集,E适于难溶于水的气体的收集,F适于能溶于水的气体的收集;
(1)①②是实验室制取气体时常用的仪器长颈漏斗和水槽;
(2)装置B适于固液不需要加热的反应,故实验室用石灰石与稀盐酸反应制取二氧化碳,应选用的发生装置是B,二氧化碳密度大于空气密度,故收集装置应选择C.
该反应的文字表达式是:碳酸钙+盐酸→氯化钙+二氧化碳+水;
(3)实验室制取二氧化碳常用石灰石和稀盐酸反应,而F中的植物油就起到避免二氧化碳和水反应的可能,影响实验的准确性;植物油上方原有的空气对实验的结果没有影响.
(4)装置A适于固体加热的反应,故实验室用高锰酸钾(KMnO4)制取氧气可选择A;氧气密度大于空气,不易溶于水就,故收集装置可选择C或E,高锰酸钾在加热条件下反应生成锰酸钾、二氧化锰和氧气,该反应的文字表达式为:高锰酸钾
锰酸钾+二氧化锰+氧气;该反应符合一变多的特点,故属于分解反应;
(5)根据质量守恒定律,化学反应前后元素的种类不变,故猜想的理由是它们都是含有氧元素的化合物;
第一组同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变,则说明二氧化锰没有分解,故猜想1错误;
第二组同学取K2MnO4在250℃条件下加热,没有用测定质量的方法,也得出了猜想Ⅱ正确的结论,该组同学选择的实验方法是制的了一些氧气;
要想验证K2MnO4受热只能部分分解,可能是生成物氧化钾(K2O)对其分解产生影响,可以设计对照实验,即取等量的锰酸钾固体于两支试管中,一支试管中加入氧化钾,一支试管中不加入氧化钾,用同样火焰的酒精灯加热,用相同规格的集气瓶,用排水法收集一瓶气体,收集一瓶氧气所用的时间作比较,确定锰酸钾的分解是否与氧化钾有关系.
故答案为:(1)长颈漏斗,水槽 (2)B,C,碳酸钙+盐酸→氯化钙+二氧化碳+水;(3)防止二氧化碳溶于水,与水反应,没有
(4)A,C或E,高锰酸钾
锰酸钾+二氧化锰+氧气,分解反应、
(5)【提出猜想】它们都是含有氧元素的化合物 ( 或:含有氧元素的物质)
【实验验证】1,制得了一些氧气
【拓展延伸】取等量的锰酸钾固体于两支试管中,一支试管中加入氧化钾,一支试管中不加入氧化钾,用同样火焰的酒精灯加热,用相同规格的集气瓶,用排水法收集一瓶气体,收集一瓶氧气所用的时间作比较,确定锰酸钾的分解是否与氧化钾有关系.
(1)①②是实验室制取气体时常用的仪器长颈漏斗和水槽;
(2)装置B适于固液不需要加热的反应,故实验室用石灰石与稀盐酸反应制取二氧化碳,应选用的发生装置是B,二氧化碳密度大于空气密度,故收集装置应选择C.
该反应的文字表达式是:碳酸钙+盐酸→氯化钙+二氧化碳+水;
(3)实验室制取二氧化碳常用石灰石和稀盐酸反应,而F中的植物油就起到避免二氧化碳和水反应的可能,影响实验的准确性;植物油上方原有的空气对实验的结果没有影响.
(4)装置A适于固体加热的反应,故实验室用高锰酸钾(KMnO4)制取氧气可选择A;氧气密度大于空气,不易溶于水就,故收集装置可选择C或E,高锰酸钾在加热条件下反应生成锰酸钾、二氧化锰和氧气,该反应的文字表达式为:高锰酸钾
| 加热 |
(5)根据质量守恒定律,化学反应前后元素的种类不变,故猜想的理由是它们都是含有氧元素的化合物;
第一组同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变,则说明二氧化锰没有分解,故猜想1错误;
第二组同学取K2MnO4在250℃条件下加热,没有用测定质量的方法,也得出了猜想Ⅱ正确的结论,该组同学选择的实验方法是制的了一些氧气;
要想验证K2MnO4受热只能部分分解,可能是生成物氧化钾(K2O)对其分解产生影响,可以设计对照实验,即取等量的锰酸钾固体于两支试管中,一支试管中加入氧化钾,一支试管中不加入氧化钾,用同样火焰的酒精灯加热,用相同规格的集气瓶,用排水法收集一瓶气体,收集一瓶氧气所用的时间作比较,确定锰酸钾的分解是否与氧化钾有关系.
故答案为:(1)长颈漏斗,水槽 (2)B,C,碳酸钙+盐酸→氯化钙+二氧化碳+水;(3)防止二氧化碳溶于水,与水反应,没有
(4)A,C或E,高锰酸钾
| 加热 |
(5)【提出猜想】它们都是含有氧元素的化合物 ( 或:含有氧元素的物质)
【实验验证】1,制得了一些氧气
【拓展延伸】取等量的锰酸钾固体于两支试管中,一支试管中加入氧化钾,一支试管中不加入氧化钾,用同样火焰的酒精灯加热,用相同规格的集气瓶,用排水法收集一瓶气体,收集一瓶氧气所用的时间作比较,确定锰酸钾的分解是否与氧化钾有关系.
点评:熟练掌握实验室中气体的制取装置的选取方法:根据反应物状态和反应条件及气体的水溶性和密度;掌握氧气的正确装置和注意点及步骤、二氧化碳的实验室制取原理和检验方法.

练习册系列答案
相关题目