题目内容
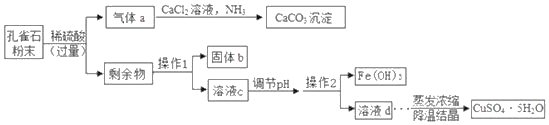
【题目】以孔雀石为原料制取胆矾(CuSO45H2O)的部分工艺流程如图所示。
(查阅资料)
I.孔雀石主要成分为Cu2(OH)2CO3,还有少量SiO2(难溶于水、不与稀硫酸反应)、Fe2O3等杂质。
Ⅱ.胆矶是一种蓝色晶体,受热易分解。
Ⅲ.在该实验条件下,Fe(OH)3、Cu(OHI)2沉淀的pH如下表:
Fe(OH)3 | Cu(OH)2 | |
开始沉淀的pH | 1.14 | 4.2 |
完全沉淀的pH | 3.0 | 6.7 |
(1)操作1的名称为_____,实验室进行该操作时玻璃棒的作用是_____。
(2)气体a生成CaCO3的同时还生成NH4C1,该反应的化学方程式为_____。
(3)溶液c中的溶质有:CuSO4、H2SO4和_____(写化学式)
(4)为将溶液中的Fe3+全部转化为Fe(OH)3,沉淀而Cu2+不转化为Cu(OH)2沉淀,应调节pH=m,m的范围是_____。
(5)获得胆矾晶体时采用降温结晶而不用蒸发结晶的主要原因是_____。
【答案】过滤 引流 CaCl2+CO2+H2O+2NH3═CaCO3↓+2NH4Cl Fe2(SO4)3 3.0≤m<4.2 防止胆矾受热分解
【解析】
(1)操作1得到的是固体和液体,所以过滤,实验室进行该操作时玻璃棒的作用是引流,从而防止液体外撒。
(2)气体a生成CaCO3的同时还生成NH4C1,是和氨气以及氯化钙反应,所以该反应的化学方程式为 CaCl2+CO2+H2O+2NH3═CaCO3↓+2NH4Cl。
(3)雀石主要成分为Cu2(OH)2CO3,还有少量SiO2(难溶于水、不与稀硫酸反应)、Fe2O3等杂质,和过量硫酸反应时,有剩余的硫酸以及生成的硫酸铜和硫酸铁,所以溶液c中的溶质的化学式为:CuSO4、H2SO4和 Fe2(SO4)3。
(4)为将溶液中的Fe3+全部转化为Fe(OH)3,沉淀而Cu2+不转化为Cu(OH)2沉淀,应调节pH=m,需要不低于氢氧化铁完全沉淀而氢氧化铜开始生成沉淀的pH,所以m的范围是 3.0≤m<4.2。
(5)获得胆矾晶体时,由于胆矾是含结晶水的化合物,为避免胆矾受热分解而失去结晶水,所以采用降温结晶而不用蒸发结晶,所以主要原因是 防止胆矾受热分解。
故答案为:
(1)过滤; 引流。
(2)CaCl2+CO2+H2O+2NH3═CaCO3↓+2NH4Cl。
(3)Fe2(SO4)3。
(4)3.0≤m<4.2。
(5)防止胆矾受热分解。

【题目】(5分)KNO3和NaCl在不同温度时的溶解度如下表所示。请回答下列问题:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |||||||||
溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | ||||||||
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | |||||||||
(1)依据上表数据,绘制出KNO3和NaCl的溶解度曲线如图所示:
图中能表示KNO3溶解度曲线的是 (填“A”或“B”)
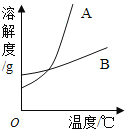
(2)由表中数据分析可知,KNO3和NaCl在某一温度时具有相同的溶解 度,则温度的范围是 ;
(3)某兴趣小组做了一下实验:
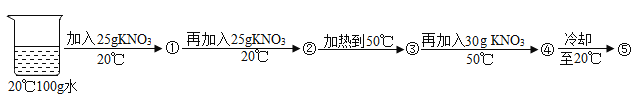
上述实验过程中得到的溶液一定属于不饱和溶液的是 (填数字序号),将⑤继续冷却至10℃,过滤,共可回收得到KNO3固体 g;
(4)硝酸钾中含有少量氯化钠时,可通过 (填“蒸发结晶”或“降温结晶”)的方法提纯。
【题目】(6分)我省两淮地区煤炭资源丰富,瓦斯存在于煤层及周围岩层中,是井下有害气体的总称,主要成分是甲烷。
(1)请你写出甲烷完全燃烧的化学方程式:__________________________________。
(2)煤矿瓦斯爆炸有两个必要条件:
①瓦斯含量在爆炸极限的范围内;②________________________________________。
(3)下表是常见三种气体的爆炸极限,请你据此判断:
最容易发生爆炸的气体是____。
可燃气体 | 爆炸极限(体积分数) |
H2 | 4.0%~74.2% |
CH4 | 5%~15% |
CO | 12.5%~74.2% |
(4)下列图标中,与燃烧和爆炸无关的是
![]()
A B C D
(5)某现代化的矿井采用了“低浓度瓦斯发电技术”,有效解决了矿区及周边地区的照明用电。这种既采煤又发电联合生产的优点是___________________________________。