题目内容
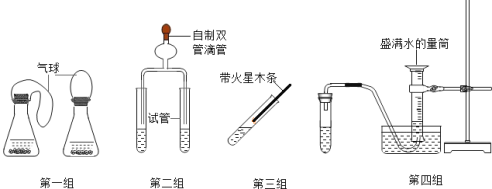
【题目】以下是一些制取气体的实验装置如图1,请你一起参与探究.
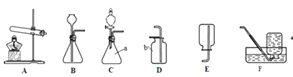
(1)写出仪器名称:a________;b________.
(2)写出实验室用A装置制氧气的化学方程式________;若要收集到浓度和纯度较高的氧气,选择的气体收集装置是________(填编号).
(3)实验室用图1中装置制取二氧化碳时,检验二氧化碳已集满的方法是________.
(4)常温下用块状电石与水反应制取乙炔气体,该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂.你认为图中最适合制取乙炔气体的发生装置是________(填编号).
(5)若选用E装置收集气体,气体应满足的条件是________.
(6)为测定某大理石样品中碳酸钙的质量分数,取某大理石样品12g于反应容器中,加入足量稀盐酸,充分反应(杂质不参与反应),产生气体质量随加入盐酸的质量的变化关系如图2所示.计算大理石样品中碳酸钙的质量分数________.

【答案】锥形瓶集气瓶2KClO3![]() 2KCl+3O2↑F将燃着的木条放到集气瓶口,若立即熄灭则集满C密度比空气小,且不与空气中的成分发生反应83.3%
2KCl+3O2↑F将燃着的木条放到集气瓶口,若立即熄灭则集满C密度比空气小,且不与空气中的成分发生反应83.3%
【解析】
(1)仪器a是锥形瓶,仪器b是集气瓶。
(2)装置A是固固加热型制取氧气的装置,且试管口没有防止棉花,故是用氯酸钾制取氧气,氯酸钾在二氧化锰做催化剂的条件下加热反应生成氯化钾和氧气,反应的方程式为:2KClO3![]() 2KCl+3O2↑。氧气的收集方法有向上排空气法和排水法,其中,向上排空气法收集的氧气较干燥,排水法收集的氧气较纯,故选F。
2KCl+3O2↑。氧气的收集方法有向上排空气法和排水法,其中,向上排空气法收集的氧气较干燥,排水法收集的氧气较纯,故选F。
(3)二氧化碳的密度比空气的密度大,不支持燃烧,也不燃烧,故检验二氧化碳是否收集满的方法是将燃着的木条放到集气瓶口,若立即熄灭则集满。
(4)制取乙炔的反应物是块状的固体和液体,反应的条件是不加热,故选固液不加热型装置,该反应需要控制液体的滴加速率从而控制反应速度,故滴加液体用分液漏斗,故选C。
(5)E装置是向下排空气法收集装置,要求被收集气体密度小于空气的密度,不能与空气反应。
(6)由图可知,12g 的大理石样品完全反应后最多生成二氧化碳的质量为4.4g,设12g 的样品中碳酸钙的质量为x

x=10g
样品中碳酸钙的质量分数为![]() ×100%=83.3%
×100%=83.3%
答;样品中碳酸钙的质量分数为83.3%。

【题目】小科同学对广口瓶产生了兴趣,在不同的实验中有着不同的作用,以下解释正确的是
实验 装置 |
|
|
|
|
解释 | 用于排空气法收集氢气的装置 | 用于干燥二氧化碳的装置 | 用于测量氧气体积的装置 | 用于医院给病人供氧气的装置 |
选项 |
|
|
|
|
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()