��Ŀ����
��7�֣�Ϊ�ۺ��������������еĸ���ƷCaSO4��ij����������������Ʊ�(NH4)2SO4�Ĺ������̣�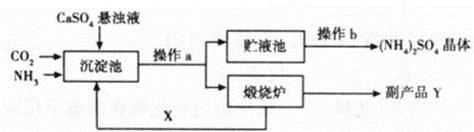
��1���������У��ڳ����ط����Ļ�ѧ��ӦΪCO2+2NH3+CaSO4+H2O==CaCO3��+ (NH4)2SO4
������¯�з����Ļ�ѧ��Ӧ����ʽΪ ���ù����п�ѭ��ʹ�õ�XΪ (�ѧʽ)������ƷY�к���; (��һ�ּ���)��
��2������Һ���л��(NH4)2SO4����Ҫ���в���b������b�� ��������һ�����������Һ���У��γ�30��ʱ(NH4)2SO4�ı�����Һ�����ʱ������������Ϊ ����֪30��ʱ����淋��ܽ��Ϊ78g����
��3�����Ʊ�6.6t (NH4)2SO4���壬��������ҪCaSO4���ٶ֣�
��1��CaCO3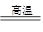 CaO+CO2�� CO2 ʳƷ�������
CaO+CO2�� CO2 ʳƷ�������
��2������ 43.8%
��3��6.8��
���������������1������¯�е�������̼��ƣ���ѧ��Ӧ����ʽΪ��CaCO3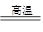 CaO+CO2�����ù����п�ѭ��ʹ�õ�XΪCO2�����и���ƷY�������ƣ���;�ǣ�ʳƷ�������
CaO+CO2�����ù����п�ѭ��ʹ�õ�XΪCO2�����и���ƷY�������ƣ���;�ǣ�ʳƷ�������
��2������Һ���л��(NH4)2SO4����Ҫ���в���b������b�ǣ�������������һ�����������Һ���У��γ�30��ʱ(NH4)2SO4�ı�����Һ����֪30��ʱ����淋��ܽ��Ϊ78g�����Դ�ʱ������������Ϊ=78g/178g��100%=43.8%
��3�����ݻ�ѧ����ʽ��CO2+2NH3+CaSO4+H2O==CaCO3��+ (NH4)2SO4��(NH4)2SO4��CaSO4��������ϵ���������CaSO4������
�⣺��CaSO4������Ϊx
CO2+2NH3+CaSO4+H2O==CaCO3��+ (NH4)2SO4
136 132
x 6.6t
136��132=x��6.6t
x=6.8t
���㣺��ѧ����ʽ����д���������������ļ��㣬���ݻ�ѧ����ʽ���㣬����ʵ�����

 �����ҵ��ٿ���������������ϵ�д�
�����ҵ��ٿ���������������ϵ�д� �»����ܶ�Ա��ϵ�д�
�»����ܶ�Ա��ϵ�д� ����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д���12�֣�ij���������к���̼������ʣ���ȡ��ϸ�ĸ���Ʒ12.4g������ƿ�У�����32.6gˮ��������γ�����Һ��������ƿ����εμ�����ʹ���ַ�Ӧ�������ݲ�������ü����������������ƿ�����ʵ�������ϵ���±���ʾ��
| �������������/g | 0 | 25 | 37.5 |
| ��ƿ�����ʵ�����/g | 45 | 70 | 80.3 |
��2����Ӧ����������̼������Ϊ����g��
��3������Ʒ���������Ƶ�����������д��������̣���ȷ��0.1%����
��18�֣���������茶�������ΪĦ���Σ���ѧʽΪxFeSO4��y(NH4)2SO4��zH2O������ҩ����Ʒ����й㷺��Ӧ�á�
���ϣ� ����������茶���������ˮ���������Ҵ���
��������ʵ��ܽ�ȣ���λ��g�����±���
| �¶�/�� | FeSO4 | (NH4) 2SO4 | xFeSO4��y(NH4)2SO4��zH2O |
| 10 | 20.0 | 73 | 17.2 |
| 20 | 26.5 | 75.4 | 21. 6 |
| 30 | 32.9 | 78 | 28.1 |
��̽��һ�����Ʊ���������茶���

ij��ȤС���ѧ���ú�������ͭ�ķ���м�Ʊ���������茶��壬�������£�
��1����ʢ�з���м�������У�������ˮ��ϴ�Ӽ�����ֽ��衣�Գ�ȥ����м��������ۣ���������ϴ�Ӽ��� ���ã�
��2���������з�����Ӧ�Ļ�ѧ����ʽΪ ��
��3����������IJ����������ձ����������� �����˲�������ֽ�ж����۷���Ϊ�˼ӿ�������ʣ���ѡ���۷��� ��

��4���������й���ʱ��Ҫ���Ƚ��е�ԭ���� �����˺�õ��Ĺ�����һ�����е������� ��
��5�������ڵ�Ŀ���ǵõ���������茶��塣����˳����b�� �� ��d��
a������ b������Ũ�� c����ȴ�ᾧ d��ϴ�Ӹ���
��6����������ʹ���Ҵ�ϴ�ӣ��ɿ������ɡ����������ŵ��� ��
A��������ˮϴ������ɵľ������
B���ƾ��ӷ����ɵ������ɾ���
��̽��������̽����������淋����
��ʵ�鲽�衿��ȡ2�ݵ���������������茶��壬�ֱ����ʵ�顣��һ���м��������NaOH��Һ����ַ�Ӧ��õ�0.68gNH3������һ���м��������BaCl2��Һ����ַ�Ӧ����ˡ�ϴ�ӡ�����õ�9.32g������
�ش��������⣺
��7��ʵ�������ɵ�NH3��ʹʪ��� ������д��(NH4)2SO4��NaOH��Ӧ�Ļ�ѧ����ʽ ������ ��Ӧ��
��8��ʵ���м������BaCl2��Һ��Ŀ�� ��
��9��ȡ���һ��ϴ��Һ������Na2SO4��Һ�� ����˵�������Ѿ�ϴ�Ӹɾ���
��10������ʵ�����ݣ�����x ��y�ı�ֵ��2�֣�д��������̣���Է���������NH3-17��BaSO4-233��
��
Ϊ��һ��ȷ����������茶������ɣ���ȡ7.84g��������茶��壬������ʹ��ֽ⣬ʣ������������¶ȵĹ�ϵ��ͼ��ʾ����

��11������ͼʾ���ݣ���������茶����У�
x��y��z = ��
��12��д��A�㵽B�㷢����Ӧ�Ļ�ѧ��
��ʽ ��