题目内容
【题目】铝是重要的轻金属,广泛应用于航空、电讯和建筑等领域。
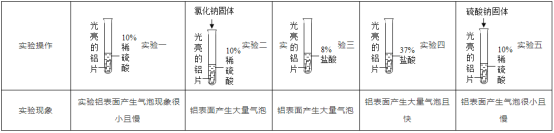
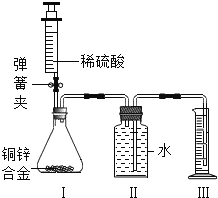
(1)依据金属的活动性顺序,铝的金属活动性比锌__________.但是将铝片和锌粒分别投入稀硫酸中,铝片表面产生的气泡却比锌粒少而慢。为了探究影响铝与酸反应速率的因素,振兴同学用相同质量、相同形状、除去氧化膜的铝片设计如图所示实验。
(2)写出实验中发生反应的化学方程式_______________________________________.
(3)比较实验三、四说明铝与酸反应产生氢气的速率,与_____________________有关.
(4)比较实验一、二说明铝与酸反应产生氢气的速率,可能与_________、_________(填粒子符号)、与和温度、金属与酸的接触面积等各种因素有关。
(5)比较实验一、二、五可以得出的结论是____________________________________.
【答案】强 2Al+3H2SO4=Al2(SO4)3+3H2↑ 盐酸浓度(或盐酸溶质质量分数) Na+ Cl- Cl-能加快酸与活泼金属的反应速率
【解析】
(1)在金属活动性顺序中,铝位于锌的前面,故活动性铝比锌强,即铝比锌活泼。
(2)铝和硫酸反应生成硫酸铝和氢气;化学方程式为:2Al+3H2SO4=Al2(SO4)3+3H2↑;
(3)比较实验三、四,除酸的浓度不同,其他因素都相同,可得出铝与酸反应产生氢气的速率与酸的浓度有关;
(4)比较实验一、二,不同之处是实验二中加入了NaCl固体,从而导致产生气泡的速率加快,因此铝与酸反应产生氢气的速率,可能与构成氯化钠的粒子--钠离子、氯离子有关;
(5)由实验一、二、五的实验现象可知,氯化钠中的氯离子可以加快金属与酸的反应速率,而硫酸钠中的硫酸根离子不能加快金属与酸的反应速率。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】水和溶液在生产、生活中起着十分重要的作用,请回答下列问题。
(1)请完成鉴别硬水和软水的实验报告。
实验步骤 | 实验现象及结论 |
___ | ___ |
(2)电解水实验装置如图甲所示,a管产生的气体是___,用燃着的木条靠近该管尖嘴处,打开活塞,可观察到的现象___。
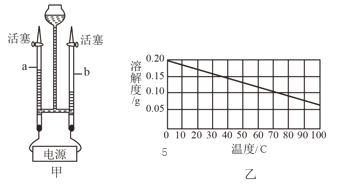
(3)图乙是氢氧化钙的溶解度曲线。40℃时,氢氧化钙的溶解度是0.14g,这句话的含义是___。将室温下的饱和氢氧化钙溶液升温(不超过100℃),发现氢氧化钙溶液变浑浊,请根据溶解度曲线解释原理:___。
(4)某石灰水含有氢氧化钙1.48g,要使该石灰水中的氢氧化钙全部转化为碳酸钙沉淀,至少需要二氧化碳的质量是_____?(请在答题纸上写出完整的解题过程)