题目内容
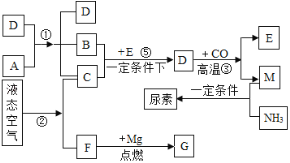
【题目】如图是某反应的微观示意图:
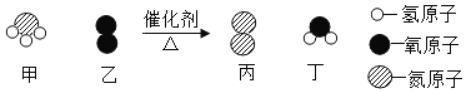
(1)写出图中单质的化学性质_____(任写一点),
(2)写出该反应的化学方程式_________________________________,
(3)反应前后化合价改变的元素是_____。
【答案】具有氧化性 4NH3+5O2![]() 4NO+6H2O 氮元素和氧元素
4NO+6H2O 氮元素和氧元素
【解析】
(1)由微粒的构成可知,图中属于单质的物质是氧气,氧气的化学性质具有氧化性等;
(2)由反应的微观示意图可知,该反应是氨气和氧气在催化剂和加热的条件下反应生成了一氧化氮和水,化学方程式为:4NH3+5O2![]() 4NO+6H2O;
4NO+6H2O;
(3)由方程式和化合价原则可知,反应前后氮元素由﹣3价变为+2价,氧元素由0价变为﹣2价,氢元素的化合价没有变化,反应前后化合价改变的元素是氮元素和氧元素。

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案
相关题目