题目内容
【题目】天然气的主要成分是甲烷(CH4),对甲烷燃烧的产物进行实验探究:
【提出问题】甲烷燃烧后生成哪些物质?
【查阅资料】含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO。
【对燃烧产物的猜想与假设】甲:CO2、H2O;乙:CO、H2O;丙:NH3、CO2、H2O;丁:CO2、CO、H2O。
你认为__________的猜想是错误的,理由是____________________________;
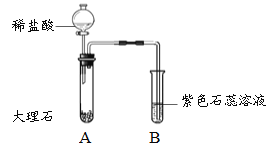
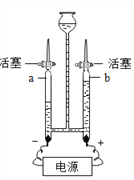
【实验探究】为了验证上述猜想与假设,将甲烷在一定量的O2中燃烧的产物依次通过下列装置:
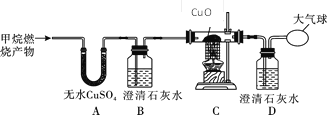
①A、B装置的顺序能否颠倒?(填“能”或“否”)________________;
②实验中观察到A中无水CuSO4变蓝,B、D中澄清石灰水变浑浊,C中黑色粉末变成红色,由此推断_________________同学的猜想成立;
③请写出A、B、C装置中发生反应的化学方程式:A._______________、B.__________________、C._________________;
【反思与交流】为避免有毒的CO污染环境,所以含碳元素的物质燃烧必须满足的条件是_______________。
【答案】 丙 反应前反应物中不含N元素,故生成物不可能有NH3(合理即可) 否 丁 CuSO4+5H2O =CuSO4.5H2O CO2+Ca(OH)2=CaCO3↓+H2O CO+CuO![]() Cu+CO2 氧气充足
Cu+CO2 氧气充足
【解析】【对燃烧产物的猜想与假设】甲烷燃烧不能生成氨气,因为反应物中不含有氮元素,所以不可能生成含有氮元素的氨气;【实验探究】①如果A、B装置的顺序颠倒,则混合气体从B中出来后,会带上水蒸气,再通过A装置时,如果无水硫酸铜变蓝色,使硫酸铜变蓝色的水可能是甲烷燃烧产生的,也可能是从石灰水中挥发出来的,也可能是二者都有,这样就影响了水的鉴别,故AB装置不能颠倒,否则无法确定甲烷燃烧产物中是否含有水;②实验中观察到A中无水CuSO4变蓝,说明甲烷燃烧生成了水;B中澄清石灰水变浑浊,说明甲烷燃烧生成了二氧化碳;D中澄清石灰水变浑浊,C中红色粉末变成黑色,说明甲烷燃烧生成了一氧化碳,由此可知,因为燃烧生成了一氧化碳、二氧化碳和水,丁同学的猜想成立;③A中无水CuSO4变蓝的化学方程式:CuSO4+5H2O=CuSO4.5H2O;B中澄清石灰水变浑浊的化学方程式:CO2+Ca(OH)2=CaCO3↓+H2O;C中黑色粉末变成红色的化学方程式:CO+CuO![]() Cu+CO2;【反思与交流】当氧气充足时,含碳元素的物质完全燃烧能生成二氧化碳,不能生成一氧化碳。
Cu+CO2;【反思与交流】当氧气充足时,含碳元素的物质完全燃烧能生成二氧化碳,不能生成一氧化碳。

 阅读快车系列答案
阅读快车系列答案