题目内容
【题目】框图中A的浓溶液在空气中会产生白雾而使浓度变低, B用于改良酸性土壤,J是最常见的金属,G是红棕色粉末,E、F、I为无色气体,I能使湿润的红色石蕊试纸变蓝。
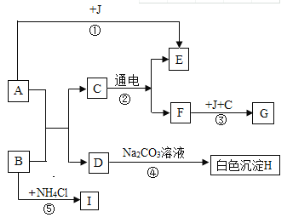
(1)写出下列物质的化学式:I_________;H________;
(2)写出反应①.⑤的化学方程式:
①__________;⑤_________;
(3)反应②的基本反应类型是________;
(4)日常生活中为了阻止反应③发生,通常采取的措施是_________;(写一条)
(5)利用反应⑤可鉴别_________和钾 肥。
【答案】NH3 CaCO3 Fe+2HCl=FeCl2+H2↑ 2NH4Cl+Ca(OH)2=CaCl2+2H2O+2NH3↑ 分解反应 保持铁制品表面干燥(或在铁制品表面喷漆、涂油、镀一层其它金属) 铵态氮肥
【解析】
A的浓溶液在空气中会产生白雾而使浓度变低,A是盐酸,B用于改良酸性土壤,B是氢氧化钙,D是氯化钙,氯化钙与碳酸钠溶液反应生成碳酸钙白色沉淀,H是碳酸钙,C在通电条件下,能发生分解反应,C是水。氢氧化钙与氯化铵反应生成氯化钙、氨气、水,I为无色气体,I能使湿润的红色石蕊试纸变蓝,I是氨气。J是最常见的金属,J是铁,铁与氧气、水反应生成铁锈,铁锈主要成分是氧化铁,氧化铁是一种红色粉末,G是红棕色粉末,则G是氧化铁,F是氧气,E是氢气。将推出的各种物质代入转化关系中进行验证,推断正确。
(1)I是NH3;H是CaCO3;
(2)反应①的化学方程式为:Fe+2HCl=FeCl2+H2↑;⑤的化学方程式为;2NH4Cl+Ca(OH)2=CaCl2+2H2O+2NH3↑
(3)反应②的化学方程式为: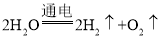 ,由一种物质发生化学反应生成两种或两种以上物质的反应是分解反应,该反应属于分解反应。
,由一种物质发生化学反应生成两种或两种以上物质的反应是分解反应,该反应属于分解反应。
(4)反应③是铁生锈,日常生活中为了阻止该反应的发生,通常采取的措施是保持铁制品表面干燥(或在铁制品表面喷漆、涂油、镀一层其它金属);
(5)含有铵根离子的物质能与碱反应生成有刺激性气味的氨气,利用反应⑤可鉴别铵态氮肥和钾肥。