题目内容
【题目】“宏观辨识与微观探析”’是化学学科核心素养之一,化学学习要让学生既能够“见微知著”,也能够“见著知微”。金属钠在氯气中燃烧生成氯化钠,右图为氯化钠形成的示意图。
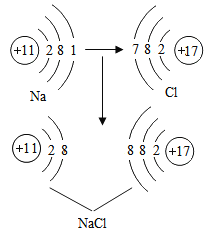
根据所给信息,请回答:
(1)钠原子的核外电子层数是 _______ ,在化学反应中易_______(填“得到”或 “失去”)电子。
(2)元素的化学性质主要是由原子的 __________________决定的。
(3)构成氯化钠的离子是________________(填微粒符号)。
【答案】3 失去 最外层电子数 Na+ 、Cl-
【解析】
(1)从钠原子的结构示意图可以得到,钠原子核外有3个电子层,故填3;
钠原子的最外层上有一个电子,在化学反应中要达到8电子稳定结构,很容易失去一个电子,使次外层变为最外层达8电子稳定结构,故填失去。
(2)最外层上的电子数决定着电子的得失,一般来说最外层电子数小于4易失去电子,使次外层变为最外层达8电子稳定结构,最外层电子数大于4较易得到电子达到最外层8电子稳定结构,因此元素的化学性质主要是由最外层上的电子数决定,故填最外层电子数。
(3)由图可知,氯化钠是由钠离子与氯离子构成的,其离子符号为Na+和 Cl-,故填Na+ 、Cl-。

练习册系列答案
相关题目