题目内容
【题目】2018年12月26日,青盐铁路正式通车了,阜宁进入了高铁时代!结合所学的知识,回答下列有关的问题:
(1)高铁列车上可提供下列食品:纯净水、食盐、橙汁、牛奶、饼干、蔗糖等。
①食盐(氯化钠)的化学式为_____;
②用化学用语表示两个水分子_____;
(2)修建铁路所需的钢铁是以铁矿石为主要原料冶炼而得的。
①磁铁矿主要成分的化学式为_____;
②炼铁时一氧化碳和赤铁矿反应的化学方程式为_____;
③雨后的铁轨表面易产生少量的锈迹,铁生锈的条件是_____,由于铁锈比较_____所以铁制品不如铝制品那样耐腐蚀。
(3)地壳中铝的含量_____(填“高于”、“ 低于”)铁,高铁车体的制造会使用大量的铝合金材料,这是因为铝合金具有耐腐蚀、硬度大、_____的特性,铝与铁相比具有很强的抗腐蚀性,其原因是铝在常温下就能与氧气反应生成 _____的氧化铝,能对内层的铝起着保护作用。
(4)以前的蒸汽列车是以燃烧煤炭来驱动的。
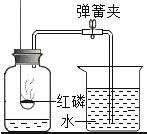
①煤炭燃烧具备的条件是:煤炭与空气(或氧气)接触且_____;
②在下列物质中,既是煤的燃烧产物,又会与空气中的水蒸汽形成酸雨的是_____;
a、二氧化碳;b粉尘;c、氮气;d、二氧化硫;e、一氧化碳;f、二氧化氮。
③煤和石油都是化石燃料,石油属于_____(填“纯净物”或“ 混合物”)。
(5)①在密闭的高铁车厢空间里,保持车厢卫生、提供清洁空气非常重要,高铁酸钠(Na2FeO4)是高铁上一种常用的消毒剂,其中铁元素的化合价为_____;
②下面是一种制备高铁酸钠的反应原理:Fe2O3+3NaNO3+4NaOH=2Na2FeO4+3NaNO2+2X。X的化学式为_____。
【答案】NaCl 2H2O Fe3O4 Fe2O3+3CO2 2Fe+3CO2 铁和氧气以及水同时接触 疏松 高于 密度小 致密 温度达到着火点 d、f 混合物 +6 H2O
2Fe+3CO2 铁和氧气以及水同时接触 疏松 高于 密度小 致密 温度达到着火点 d、f 混合物 +6 H2O
【解析】
本题考查的基础知识点较多,主要有化学用语的书写及常见物质的结构、性质与用途。
(1)①食盐(氯化钠)的化学式为 NaCl;
②用化学用语表示两个水分子2H2O。
(2)①磁铁矿主要成分的化学式为Fe3O4;
②炼铁时一氧化碳和赤铁矿反应的化学方程式为Fe2O3+3CO2![]() 2Fe+3CO2;
2Fe+3CO2;
③铁生锈的条件是铁和氧气以及水同时接触,由于铁锈比较疏松所以铁制品不如铝制品那样耐腐蚀。
(3)地壳中铝的含量高于铁,高铁车体的制造会使用大量的铝合金材料,这是因为铝合金具有耐腐蚀、硬度大、密度小的特性,铝与铁相比具有很强的抗腐蚀性,其原因是铝在常温下就能与氧气反应生成致密的氧化铝,能对内层的铝起着保护作用。
(4)①煤炭燃烧具备的条件是:煤炭与空气(或氧气)接触且温度达到着火点;
②二氧化硫、二氧化氮既是煤的燃烧产物,又会与空气中的水蒸汽形成酸雨,故填:d、f;
③煤和石油都是化石燃料,石油属于 混合物。
(5)①利用化合物中正负化合价代数和为零的原则,可求出(Na2FeO4)中铁元素的化合价为+6。
②根据质量守恒定律在化学反应前后原子种类和个数不变,可推知Fe2O3+3NaNO3+4NaOH=2Na2FeO4+3NaNO2+2X中X的化学式为H2O。

 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案【题目】在实验课中,各小组作了如下实验:
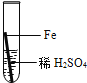
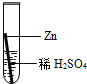
实验编号 | 1 | 2 | 3 | 4 |
实验操作 |
|
|
|
|
实验后,同学们按老师要求将废液都倒在指定的大烧杯中,小科猜想该烧杯中的废液可能有硫酸铜、硫酸锌、硫酸亚铁......应该可以从中提炼出铁和铜。经思考后,他设计了如图所示的实验,并设法使滤液甲和乙所含的溶质相同。
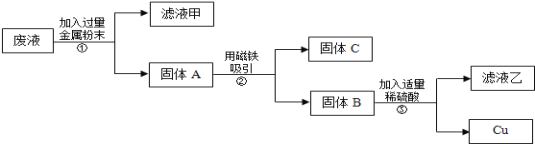
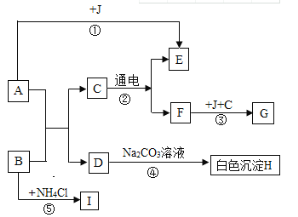
(1)则固体C是_____,操作③的名称是_____;
(2)操作③的化学方程式是_____;反应类型是_____。