题目内容
【题目】硫酸和盐酸是实验室常用的试剂。请回答下列问题:
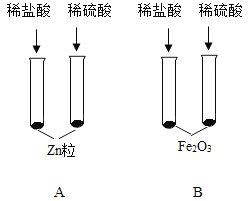
(1)A组试管中都产生H2,若要制得较纯的H2,选稀硫酸而不选盐酸的原因是:_____。
(2)B组试管中实验现象相同,该现象是_____。右侧试管的反应的化学方程式为_____。
(3)鉴别稀硫酸和盐酸的试剂是_____。
【答案】盐酸有挥发性(或盐酸挥发出氯化氢气体使制得的氢气中混有氯化氢气体) 红色固体逐渐溶解,溶液由无色变成黄色 Fe2O3+3H2SO4=Fe2(SO4)3+3H2O 硝酸钡溶液(合理即可)
【解析】
(1)盐酸有挥发性,挥发出来的氯化氢气体使制得的氢气中混有氯化氢气体,会影响氢气的纯度,故填盐酸有挥发性(或盐酸挥发出的氯化氢气体使制得的氢气中混有氯化氢气体)。
(2)氧化铁与盐酸反应生成氯化铁和水,与硫酸反应生成硫酸铁和水,氯化铁与硫酸铁均溶于水,且水溶液均呈黄色,所以观察到的现象是红色固体逐渐溶解,溶液由无色变成黄色,故填红色固体逐渐溶解,溶液由无色变成黄色;
右侧试管中的反应是氧化铁与硫酸反应生成硫酸铁与水,故反应的化学方程式写为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O。
(3)稀硫酸和盐酸中的酸根离子不同,区别两种溶液时,可向两种溶液中滴加硝酸钡溶液,产生白色沉淀的是稀硫酸,无明显变化的是盐酸,故填硝酸钡溶液。

【题目】做完加热铜片的实验后,小明同学对其成分进行分析。取10g此样品,向其中分五次加入相同溶质质量分数的稀硫酸,使之充分反应,每次所用稀硫酸的质量及剩余固体的质量记录于下表:
第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
加入稀硫酸的质量/g | 20 | 20 | 20 | 20 | 20 |
充分反应后剩余固体的质量/g | 9.2 | 8.4 | 7.6 | 7 | 7 |
试回答下列问题:
(1)10g样品中氧化铜的质量为__________g。
(2)计算所加入稀硫酸中溶质的质量分数____________________。