题目内容
【题目】向CuSO4溶液中加入一定量NaHCO3,产生大量气泡和绿色固体,溶液逐渐变为无色。
(1)将产生的气体通入澄清石灰水,变浑浊,则该气体为__________。
(2)某同学经过滤、洗涤等操作得到绿色固体和无色溶液,并进行如下探究。
[资料]常见绿色固体有碱式碳酸铜[Cu2(OH)2CO3]和碱式硫酸铜[Cu4(OH)6SO4],都不溶于水,但能与酸反应。Na2SO4固体受热不易分解。
I.绿色固体成分的探究
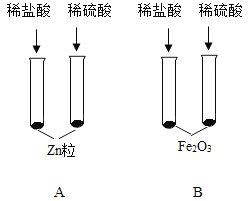
[实验1]取洗净后的绿色固体,加入足量的_________溶液,产生大量气泡,振荡后滴加___________,无现象,则该固体只含碱式碳酸铜。
II.溶液成分的探究
[猜测]取一定量溶液经蒸发、低温干燥等操作得到白色固体,作如下猜测:白色固体可能是:①Na2SO4 ②NaHCO3 ③Na2SO4和NaHCO3
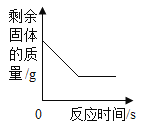
[实验2]取该白色固体8.4g充分加热至质量不再改变为止,测得剩余固体的质量_______( 选填“<”、“=”或“>”)5.3g,则猜测①、②、③都不成立。
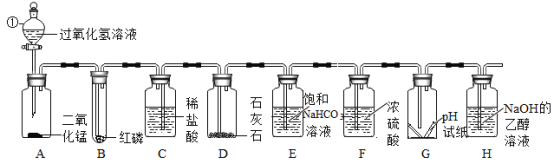
[实验3]有同学查阅资料得知上述固体应为Na2SO410H2O和NaHCO3的混合物。为进一步确定白色固体的组成,该同学取适量白色固体,充分加热至质量不再改变,并使产生的气体全部缓缓通过下图_______(选填 “甲”或“乙”)装置,测定生成气体的质量。
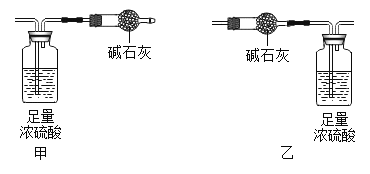
[数据]①浓硫酸增重2.7g;②碱石灰增重2.2g。则固体中各成分的质量比为_____________。
[结论]写出CuSO4溶液和NaHCO3溶液反应的化学方程式_____________。
【答案】CO2 稀盐酸或稀硝酸 BaCl2或Ba(NO3)2溶液 < 甲 161:420或420:161 ![]()
【解析】
(1)二氧化碳能使澄清石灰水变浑浊,故该气体为二氧化碳;
I、绿色固体成分的探究
实验1:结论为该固体中只含碱式碳酸铜,故取洗净后的绿色固体,加入足量的稀盐酸溶液,稀盐酸与碱式碳酸铜反应,生成氯化铜、二氧化碳和水,故产生大量气泡,振荡后滴加氯化钡溶液,无现象,则该固体只含碱式碳酸铜,因为碱式硫酸铜与稀盐酸反应生成氯化铜、硫酸铜和水,氯化钡能与硫酸铜反应生成硫酸钡沉淀,故填:稀盐酸、氯化钡;
Ⅱ、溶液成分的探究
实验2:假设该8.4g白色固体是碳酸氢钠,设完全反应生成碳酸钠的质量为x
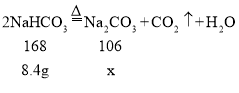
![]() ,x=5.3g
,x=5.3g
如果剩余固体的质量等于5.3g,则该白色固体为碳酸氢钠,如果大于5.3g,则该白色固体是碳酸氢钠和硫酸钠的混合物,如果剩余固体的质量等于8.4g,则该白色固体是硫酸钠,故充分加热至质量不再改变为止,测得剩余固体的质量<5.3g,则猜测①、②、③都不成立;
实验3:应使产生的气体全部缓缓通过甲装置,通过浓硫酸,测定生成水的质量,通过碱石灰测定生成二氧化碳的质量,如果通过乙装置,则无法分别测定水和二氧化碳的质量;
数据:①浓硫酸增重2.7g,②碱石灰增重2.2g,说明共生成了2.7g水,2.2g二氧化碳,设碳酸氢钠的质量为x,碳酸氢钠加热生成水的质量为y
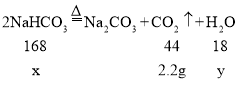
![]() ,
,![]()
x=8.4g,y=0.9g
Na2SO410H2O中水的质量为:2.7g-0.9g=1.8g
Na2SO410H2O的质量为:![]()
故固体中NaHCO3和Na2SO410H2O的质量比为:8.4g:3.22g=420:161;
结论:由分析可知,硫酸铜溶液与碳酸氢钠溶液反应生成碱式碳酸铜、Na2SO4、二氧化碳和水,该反应的化学方程式为:![]() 。
。

 精英口算卡系列答案
精英口算卡系列答案【题目】某小组用图表对所学知识进行归纳,其中甲包含乙和丙,不包含丁(如图所示)。下列表格中的各组物质或变化符合这种关系的是( )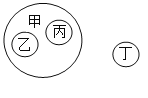
选项 | 甲 | 乙 | 丙 | 丁 |
A | 化合物 | 盐酸 | MnO2 | 铁粉 |
B | 合成材料 | 合金 | 合成纤维 | 合成橡胶 |
C | 化学变化 | 置换反应 | 化合反应 | 复分解反应 |
D | 放热反应 | 硫在空气中燃烧 | NaOH溶液与稀H2SO4反应 | 高温分解石灰石 |
A.AB.BC.CD.D