题目内容
【题目】肥料是农业生产中必不可少的,已知某氮肥溶液可能是氯化铵、碳酸铵、硫酸铵、尿素中的一种或几种,现要检验其成分,进行如下实验:
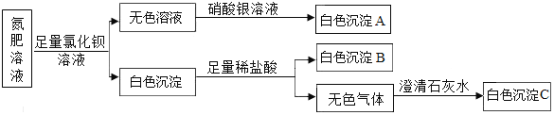
(1)写出产生沉淀C的化学方程式___________。
(2)通过以上实验分析,该氮肥溶液中一定含有哪些物质___________?
(3)选用哪种试剂代替氯化钡溶液,能检测出可能含有的一种氮肥是否存在___________。
【答案】CO2+Ca(OH)2=CaCO3↓+H2O 碳酸铵和硫酸铵 硝酸钡溶液
【解析】
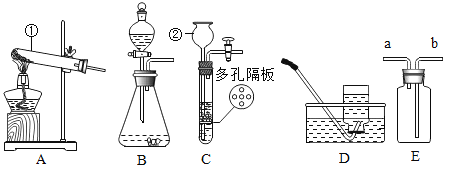
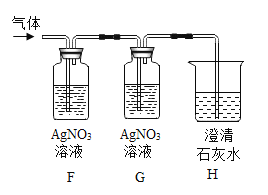
氮肥溶液加入足量氯化钡溶液生成白色沉淀,白色沉淀与足量稀盐酸反应后生成无色气体和白色沉淀B,说明白色沉淀部分溶于稀盐酸,则白色沉淀应该是碳酸钡与硫酸钡的混合物,其中的碳酸钡与稀盐酸反应生成的无色气体是二氧化碳,二氧化碳与澄清石灰水中的氢氧化钙反应生成碳酸钙沉淀和水。
(1)由分析可知,白色沉淀C是碳酸钙,生成沉淀C的反应是二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,故反应的化学方程式写为:CO2+Ca(OH)2=CaCO3↓+H2O。
(2)由分析可知,加入足量氯化钡溶液后生成的白色沉淀是碳酸钡与硫酸钡的混合物,根据质量守恒定律可知,氮肥溶液中一定含有碳酸根离子与硫酸根离子,所以该氮肥溶液中一定含有碳酸铵和硫酸铵,故填碳酸铵和硫酸铵。
(3)实验中先向氮肥溶液中加入氯化钡溶液,再向溶液中加入硝酸银溶液产生白色沉淀A,白色沉淀A为氯化银,由于氯化钡溶液中含有氯离子,所以无法确定氮肥溶液中是否含有氯离子,进而无法判断氯化铵是否存成,为避免氯化钡中的氯离子对检验氯化铵的存在产生干扰,可用硝酸钡溶液代替氯化钡溶液进行试验来确定氯化铵是否存在,故填硝酸钡溶液。

【题目】工业上常利用电石制乙炔气体![]() 时产生的灰浆和残渣制备化工原料
时产生的灰浆和残渣制备化工原料![]() 和超细
和超细![]() .
.
![]() 电石制乙炔气体
电石制乙炔气体![]() 时产生灰浆和残渣的过程如下:电石
时产生灰浆和残渣的过程如下:电石![]() 灰浆
灰浆![]() 残渣,其中电石与水反应生成氢氧化钙和乙炔,写出该反应的化学方程式 ______,残渣中主要成分是
残渣,其中电石与水反应生成氢氧化钙和乙炔,写出该反应的化学方程式 ______,残渣中主要成分是![]() 和 ______ .
和 ______ .
Ⅰ![]() 制备
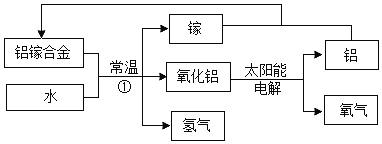
制备![]() 的流程如图:
的流程如图:
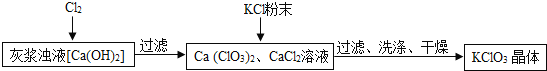
![]() 向灰浆浊液中通入
向灰浆浊液中通入![]() ,得到
,得到![]() 、
、![]() 溶液.反应中
溶液.反应中![]() 与
与![]() 的化学计量数分别为1和
的化学计量数分别为1和![]() 写出此反应的化学方程式 ______ .
写出此反应的化学方程式 ______ .
![]() 有关物质在常温下的溶解度如下:
有关物质在常温下的溶解度如下:
物质 |
|
|
| KCl |
溶解度 |
|
|
|
|
上述流程中加入KCl粉末,KCl与 ______ ![]() 填化学式
填化学式![]() 发生了复分解反应,得到
发生了复分解反应,得到![]() 晶体.你认为能得到
晶体.你认为能得到![]() 晶体的原因是 ______ .
晶体的原因是 ______ .
![]() 洗涤时,可选用下列洗涤剂 ______
洗涤时,可选用下列洗涤剂 ______ ![]() 填字母编号
填字母编号![]() .
.
A KCl饱和溶液![]() 冰水
冰水![]() 饱和
饱和![]() 溶液
溶液
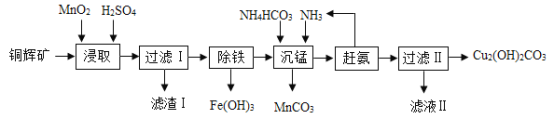
Ⅱ![]() 制备超细
制备超细![]() 的流程如下
的流程如下![]() 注:加入
注:加入![]() 溶液的目的是溶解残渣中的难溶盐
溶液的目的是溶解残渣中的难溶盐![]() :
:
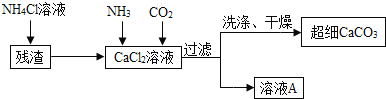
![]() 向
向![]() 溶液中通入两种气体,生成超细
溶液中通入两种气体,生成超细![]() 的化学方程式 ______
的化学方程式 ______ ![]() 检验
检验![]() 是否洗涤干净的方法是 ______ .
是否洗涤干净的方法是 ______ .
![]() 流程中溶液A可循环使用,其主要成分的化学式是 ______ .
流程中溶液A可循环使用,其主要成分的化学式是 ______ .
【题目】某同学发现,上个月做实验用的NaOH溶液忘记了盖瓶盖.对于该溶液是否变质,同学们开始实验探究.
(猜想假设)
猜想(1):该溶液没有变质,为NaOH溶液.
猜想(2):该溶液全部变质,为Na2CO3溶液.
猜想(3):该溶液部分变质,为NaOH和Na2CO3的混合溶液.
(查阅资料)Na2CO3溶液呈碱性
(设计方案)请你完善下表几组同学探讨的设计方案
实验操作 | 可能出现的现象与结论 | 同学评价 | |
第1组 |
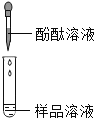
| 若溶液变红,则猜想(2)不成立 | 第2组同学认为:此方案结论不正确,理由是:__. |
第2组 |
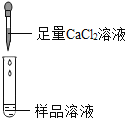
| 若产生白色沉淀,反应方程式是:_____ 则猜想(1)不成立. | 第3组同学认为:此方案还不能确定猜想(2)还是猜想(3)成立. |
第3组 |
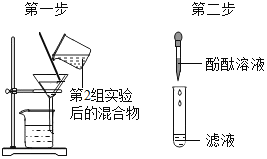
| 若滤液不变红,则猜想(2)成立;若滤液变红,则猜想(3)成立. | 第1组同学认为:不需过滤也能达到实验目的,更简单的操作方法是:_____ |
(探究实验)综合各小组的方案后,动手实验.
(结论与反思)(1)NaOH溶液易与空气中_____反应而变质,为防止变质,所以保存时要_____.
(2)第二组实验中,产生沉淀的方程式为:_____.