题目内容
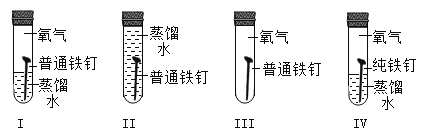
【题目】化学兴趣小组做盐的化学性质实验,如图所示。
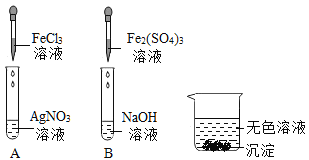
甲同学用试管取少量A中反应后的上层清液,向试管中加入少量稀盐酸,无变化。
(1)乙同学将A、B两试管内反应后的物质过滤,将滤液依次倒入烧杯中,观察到如图所示现象。烧杯中一定发生反应的化学方程式为________。
(2)小组同学对烧杯溶液中所含离子成分产生兴趣。
(提出问题)烧杯的溶液中含有什么离子?
(猜想与假设)甲猜想:Na+、SO42-和NO3-
乙猜想:Na+、SO42-、NO3-和Cl-
丙猜想:________
(3)(活动与探究)甲同学的实验方案如下:用试管取少量烧杯中溶液,向溶液中加入足量的Ba(NO3)2和稀硝酸的混合溶液,若观察到有白色沉淀产生,则证明溶液中有SO42-。你认为他的方案________(填“是”或“否”)正确。
乙同学另取一只试管取少量烧杯中的溶液,向试管中先依次加入________两种溶液,最后再加入AgNO3溶液,均观察到相同的实验现象。小组同学根据上述实验现象得出了正确结论。烧杯溶液中含有的离子是________。
(4)(总结与反思)通过三位同学的实验可以得出:溶液中的待测离子不是一种,且有干扰离子存在时,可以选择适当的试剂依次加入,对于先加入的试剂除了要有明显的实验现象外,还需要考虑的问题及目的是________,最后一种加入的试剂只需考虑有明显现象即可。
【答案】3NaOH+Fe(NO3)3=Fe(OH)3↓+3NaNO3 Na+、SO42-、NO3-、OH-或Na+、SO42-、NO3-、OH-、Cl- 是 足量Ba(NO3)2、足量Mg(NO3)2或足量Mg(NO3)2、足量Ba(NO3)2 Na+、SO42-、NO3-、OH-、Cl- 要足量,目的是将存在的待测离子、干扰离子除去(尽)以免影响后面的待测离子的检验。合理即可
【解析】
氯化铁和硝酸银反应生成氯化银和硝酸铁,硫酸铁和氢氧化钠反应生成氢氧化铁和硝酸钠,氢氧化钠和硝酸铁反应生成氢氧化铁和硝酸钠。
(1)甲同学用试管取少量A中反应后的上层清液,向试管中加入少量稀盐酸,无变化,说明A中无硝酸银剩余,乙同学将A、B两试管内反应后的物质过滤,将滤液依次倒入烧杯中,有无色溶液和沉淀生成,说明B中有氢氧化钠剩余,沉淀为氢氧化铁沉淀,烧杯中一定发生反应的方程式为3NaOH+Fe(NO3)3=Fe(OH)3↓+3NaNO3。
(2)烧杯中一定存在的溶质为硝酸钠和硫酸钠,为无色溶液,可能是氢氧化钠剩余,若A中有氯化铁剩余,可能生成氯化钠,溶液中离子可能是钠离子、硫酸根离子、硝酸根离子和氢氧根离子或钠离子、硫酸根离子、硝酸根离子、氢氧根离子和氯离子,故丙猜想:Na+、SO42-、NO3-、OH-或Na+、SO42-、NO3-、OH-、Cl-。
(3)用试管取少量烧杯中溶液,向溶液中加入足量的Ba(NO3)2和稀硝酸的混合溶液,若观察到有白色沉淀产生,说明有硫酸钡沉淀生成,则证明溶液中有SO42-,故他的方案是正确的。
乙同学要证明结论,要通过加入足量的硝酸钡溶液和硝酸镁溶液证明硫酸根离子和氢氧根离子的存在,并除去两种离子,然后再加入硝酸银溶液,证明氯离子是否存,都观察到相同的实验现象,即产生白色沉淀,说明离子成分为 Na+、SO42-、NO3-、OH-、Cl-。
(4)对于先加入的试剂除了要有明显的实验现象外,还需要考虑的问题及目的是用量必须保证将有干扰的离子全部除去,以免影响后面的待测离子的检验。

【题目】在宏观、微观和符号之间建立联系是化学学科学习的特点。
(1)甲、乙、丙、丁表示四种物质,它们的微观示意图如表所示:
物质 | 甲 | 乙 | 丙 | 丁 |
|
微观示意图 |
|
|
|
|
①一个丙分子共有___________个原子。
②甲、乙、丙、丁四种物质中属于氧化物的是__________和____________(写化学式)。
(2)工业上使用一种国产低温催化剂生产氢气的反应过程如图所示:
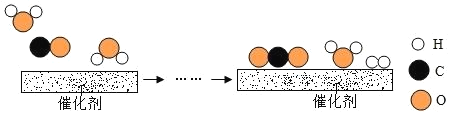
①该反应的化学方程式为_______________;
②参加反应的![]() 与
与![]() 分子个数之比为______________。
分子个数之比为______________。