题目内容
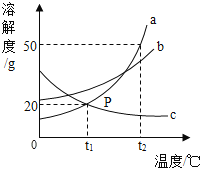
【题目】下列所示的四个图像,能正确反映对应变化关系的是
A.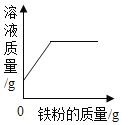 向一定量的硝酸铜和硝酸镁的混合溶液中加入铁粉
向一定量的硝酸铜和硝酸镁的混合溶液中加入铁粉
B.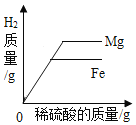 等质量的镁和铁分别与等质量、等浓度足量的稀硫酸反应
等质量的镁和铁分别与等质量、等浓度足量的稀硫酸反应
C.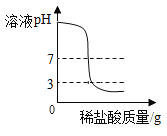 向一定量的氢氧化钠溶液中 滴加pH=3的稀盐酸
向一定量的氢氧化钠溶液中 滴加pH=3的稀盐酸
D.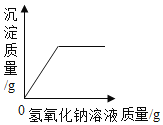 向一定量的含有 盐酸的氯化铜溶液中滴加氢氧化钠溶液
向一定量的含有 盐酸的氯化铜溶液中滴加氢氧化钠溶液
【答案】B
【解析】
A、铁的金属活动性比铜强,比镁弱,向一定量的硝酸铜和硝酸镁的混合溶液中加入铁粉,铁不能与硝酸镁溶液反应,铁能与硝酸铜溶液反应生成硝酸亚铁溶液和铜,参加反应的铁的质量小于生成铜的质量,则溶液的质量应减少,故错误;
B、等质量的镁和铁分别与等质量、等浓度足量的稀硫酸反应,横坐标是硫酸的量,故等量的硫酸产生氢气的质量相等,当金属全部参加反应,生成氢气的质量与金属的相对原子质量成反比(+2价的金属),则镁产生的氢气的质量大于铁,故正确;
C、向一定量氢氧化钠溶液中滴加pH=3的稀盐酸,稀盐酸和氢氧化钠反应生成氯化钠和水,随着反应进行,溶液碱性减弱,pH减小,恰好完全反应时pH=7,继续加入稀盐酸时,溶液pH小于7,但是不能减小到3,更不能小于3,故错误;
D、向含有盐酸的氯化铜溶液中滴加烧碱溶液时,氢氧化钠先和稀盐酸反应,后和氯化铜反应,因此开始不能产生沉淀,故错误。
故选:B。

 阅读快车系列答案
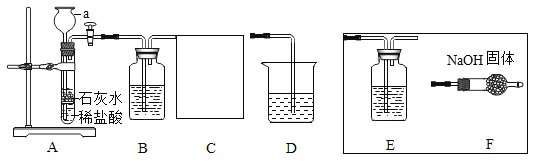
阅读快车系列答案【题目】在20℃环境中,制取干燥的二氧化碳气体,并验证二氧化碳气体与氢氧化钠溶液可以发生化学反应,设计如图探究实验。
(查阅资料)
(1)碳酸钠、水、二氧化碳可以化合生成碳酸氢钠。
(2)20℃,氢氧化钠、碳酸钠和碳酸氢钠的溶解度如下表所示:
物质 | 氢氧化钠 | 碳酸钠 | 碳酸氢钠 |
溶解度/g | 110 | 21.8 | 9.6 |
(定性探究)
(1)装置F中导管外的玻璃仪器名称是_____。
(2)装置B中盛有碳酸氢钠溶液,目的是吸收装置A中挥发出的氯化氢气体,写出B中发生反应的化学方程式:_____。
(3)装置C的作用是_____,选择_____(选填E、F)装置达到实验目的。
(4)在实验过程中装置D中观察到_____,说明二氧化碳和氢氧化钠溶液能发生化学反应。
【题目】如图所示装置(气密性良好),若先将甲中液体滴入丙中,观察到气球明显鼓起,一段 时间后恢复到原状;再将乙中液体滴入丁中,气球又明显鼓起。下列组合正确的是( )
选项 | 滴管甲 | 烧杯丙 | 滴管乙 | 烧杯丁 |
A | 过氧化氢溶液 | 二氧化锰 | 水 | 氯化钠 |
B | 稀硫酸 | 锌 | 盐酸 | 碳酸钠 |
C | 水 | 氢氧化钠 | 水 | 硝酸铵 |
D | 水 | 氧化钙 | 盐酸 | 镁 |
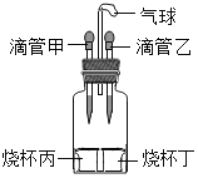
A. AB. BC. CD. D
【题目】某实验小组为探究酸的化学性质,由甲、乙、丙同学设计并完成了如图所示的实验。
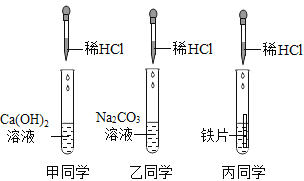
(1)甲同学实验中所发生反应的化学方程式为______________。丙同学实验试管中的反应现象为______________。
[在阅资料] CaCl2、NaCl 的溶液是中性,Na2CO3溶液显碱性。
[实验报究一 ]确定甲、乙同学上述实验后所得溶液中的溶质。
(2)取甲所得溶液少许,加入石蕊试液,溶液显红色,甲所得溶液中一定含有的溶质是_____________(写化学式)
(3)取乙所得溶液少许,加入酚酞试液,溶液显红色,乙所得溶液中一定含有的溶质是______________。(写化学式)
[实验探究二]确定甲、乙同学上述实验所得溶液混合后的成分。
(4)甲、乙同学把上述实验所得溶液倒入同一废液缸中,观察到先有气泡产生,后有白色沉淀生成。同学们将烧杯内的物质进行过滤,对所得滤液的溶质成分进行探究。
甲同学猜想: NaCl;
乙同学猜想:NaC1、CaCl2;
丙同学猜想: NaCl、CaCl2、HCl;
你的猜想:______________。
[交流讨论]
(5)你认为_____________同学的猜想一 定不正确, 理由是______________。
[设计实验]请设计实验证明你的猜 想正确。
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,向其中滴加_____________。 | ______________。 | 猜想成立。 |