题目内容
【题目】下图所示为实验室中常见的气体制备、干燥、收集和性质实验的部分仪器。(组装实验装置时,可重复选择仪器) 试根据题目要求,回答下列问题:
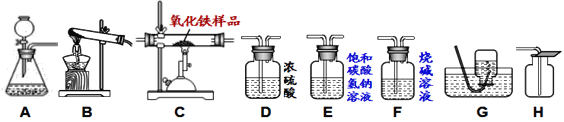
⑴小庆同学以石灰石和稀盐酸为原料,在实验室欲制备并收集一瓶干燥、纯净的CO2气体。他按照要求设计了实验装置,连接仪器并检验装置的气密性,制取气体。(提示:挥发出的少量HCl气体可用饱和碳酸氢钠溶液吸收)。
①他所选仪器的连接顺序应为____________(填写仪器序号字母)。
②装置A中发生反应的化学方程式为_________________________。
③证明CO2已收集满的方法:_____________________。
⑵小颖同学欲用CO气体测定某氧化铁样品中所含Fe2O3的质量分数(假设杂质不挥发,也不发生反应),仪器的连接顺序为: 一氧化碳 → C → F → 燃着的酒精灯 。
①装置C处发生反应的化学方程式为__________,该装置中可观察到的实验现象为___________。
②若一氧化碳中含有少量二氧化碳,则通过测量反应前后装置F的增重,来测算氧化铁样品中所含Fe2O3的质量分数,则测算结果将_________(填“偏小”、“偏大”、“不受影响”之一)。
③若实验过程中不进行尾气处理,逸出的CO气体会危害人身安全,并污染空气。下列有关煤气(主要成分CO)的说法中,正确的是__________(填序号)。
A.在有煤炭炉的室内放置一盆水,可防止煤气中毒
B.发现室内有人煤气中毒时,应立即开灯检查并用手机打急救电话
C.发现有人煤气轻微中毒时,应速将病人移到通风良好、空气新鲜的地方
D.点燃一氧化碳气体前,必须先检验其纯度
【答案】 A→E→D→H CaCO3 + 2HCl CaCl2 + H2O + CO2↑ 将一根燃着的木条放在瓶口,若其熄灭,则说明CO2已集满 3CO + Fe2O3 高 温 2Fe + 3CO2 红色固体逐渐变黑色 偏大 CD
【解析】(1)①制取二氧化碳用固液不加热型装置A,由于制得的气体中混有氯化氢气体,需要经过装置E 除去氯化氢气体,后经装置D除去水分,后有向上排空气法装置H收集,故顺序为 A→E→D→H
②装置A中发生反应是稀盐酸与碳酸钙反应生成氯化钙、二氧化碳和水,反应的化学方程式为CaCO3 + 2HCl=CaCl2 + H2O + CO2↑。
③证明CO2已收集满的方法是将一根燃着的木条放在瓶口,若其熄灭,则说明CO2已集满;
(2)①装置C处发生反应是氧化铁与一氧化碳反应生成铁和二氧化碳,反应的化学方程式为3CO + Fe2O3 高 温 2Fe + 3CO2 ;该装置中可观察到的实验现象为红色固体逐渐变黑色。
②若一氧化碳中含有少量二氧化碳,则F装置中质量增加量偏大,故测量结果偏大;
③A.一氧化碳难溶于水,故在有煤炭炉的室内放置一盆水,不能防止煤气中毒,错误;
B.发现室内有人煤气中毒时,如立即开灯检查可能引起爆炸,错误;
C.发现有人煤气轻微中毒时,应速将病人移到通风良好、空气新鲜的地方,正确;
D.点燃一氧化碳气体前,必须先检验其纯度,正确。故选CD 。

 智能训练练测考系列答案
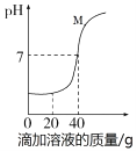
智能训练练测考系列答案【题目】某化学兴趣小组为了测定镁铜合金中镁的质量分数,取了该合金样品2.0g并将30稀硫酸分6次加入样品中。充分反应后过滤,称重,得到相关数据如下:
稀硫酸的用量 | 剩余固体质量 | 稀硫酸的用量 | 剩余固体质量 |
第一次 5 g | m | 第四次 5 g | 0.8 g |
第二次 5 g | 1.4g | 第五次 5 g | 0.6g |
第三次 5 g | 1.1g | 第六次 5 g | 0.6g |
(1) 表格中m的数值为________。
(2) 样品中镁的质量分数为________。
(3) 求所用硫酸溶液中溶质质量分数为_____________。