题目内容
【题目】利用稀盐酸与NaOH溶液探究中和反应时,采用传感器测量烧杯中溶液pH的变化情况(如图所示)。下列说法正确的是
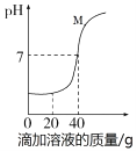
A. 该实验是将稀盐酸滴入NaOH溶液中
B. 滴加溶液为20 g时,反应放出的热量最多
C. 滴加溶液为40 g时,烧杯内的溶液不能导电
D. M点对应溶液中的溶质是NaCl和NaOH
【答案】D
【解析】A.根据图象中pH值的变化是从小于7逐渐的增大到大于7,进行分析解答;
B.根据中和反应是否反应完分析;
C.溶液是否导电主要取决于溶质在溶剂中是否以离子形式存在;
D. 根据M点的pH大于7,溶液显碱性,据此进行分析判断。
解:A.由图象可知,pH值是开始时小于7逐渐的增大到7然后大于7,可知原溶液显酸性,然后不断的加入碱性溶液,使pH增大,说明是把氢氧化钠滴加到稀盐酸溶液中,故错误;
B. 滴加溶液为20 g时,此时反应为结束,故错误;
C. 滴加溶液为40 g时,此时氢氧化钠与稀盐酸恰好好中和,溶液是氯化钠溶液,溶液中氯化钠以氯离子和钠离子形式存在,故此时烧杯中的溶液能导电,因此错误;
D. M点的pH大于7,溶液显碱性,说明滴加氢氧化钠溶液过量,故溶质是NaCl和NaOH,正确。

练习册系列答案
相关题目
【题目】除去下列各组物质中少量的杂质,所用试剂或方法正确的是
选项 | 物质 | 杂质 | 除杂所用试剂或方法 |
A. | CO2 | CO | 点燃 |
B. | Ag粉 | Mg粉 | 适量稀硫酸 |
C. | NaOH溶液 | Na2CO3 | 适量稀盐酸 |
D. | NaCl | KNO3 | 冷却结晶 |
A. A B. B C. C D. D