题目内容
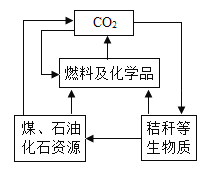
【题目】现有初中化学常见的物质A~G,其中C为常用的食品干燥剂的主要成分,它们之间存在如下图所示关系。下列说法错误的是
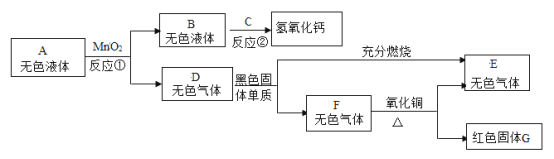
A.反应①可用于实验室制取氧气
B.反应②的化学方程式:CaO+H2O=Ca(OH)2
C.气体E不支持燃烧,可用于灭火
D.红色固体G可由金属Ag与CuSO4溶液直接反应得到
【答案】D
【解析】
C是食品干燥剂的主要成分,而且能转化为氢氧化钙,则C可能是氧化钙。氧化钙和无色液体B反应能够转化为氢氧化钙,则B可能是水。无色液体A在二氧化锰的催化作用下能分解出水和无色气体D,则A可能是过氧化氢溶液,D可能是氧气。黑色固体在氧气中充分燃烧和不充分燃烧会生成不同的物质,则该黑色固体可能是碳,充分燃烧生成的无色气体E可能是二氧化碳,无色气体F可能是一氧化碳。一氧化碳还原氧化铜,生成红色固体G和无色气体E,则红色固体G是铜。
将推测带入题中,符合题意,推断正确。
A、反应①是过氧化氢在二氧化锰的催化作用下分解出水和氧气。该反应可以用于实验室制取氧气。故A说法正确;
B、反应②指的是氧化钙和水反应生成氢氧化钙。其化学方程式为:CaO+H2O=Ca(OH)2。故B说法正确;
C、气体E是二氧化碳,二氧化碳不燃烧不支持燃烧,可以用于灭火。故C说法正确;
D、红色固体G是铜。银和硫酸铜不会发生化学反应,无法置换出硫酸铜中的铜,所以无法直接制得。故D说法错误。
故选D。

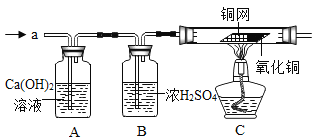
【题目】常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体。小明设计如下实验探究铁粉与水蒸气领反应后的产物。

(1)试管尾部放一团湿棉花的目的是_____。
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂液肥皂泡飘到空中。说明生成的气体是_____。
(3)探究试管中剩余固体成分是什么?
(查阅资料)
常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被磁铁吸引 | 否 | 否 | 能 |
化学性质 | 能溶于酸液但不产生气体,不用溶于硫酸铜溶液 | ||
(初步验证)试管中剩余固体为黑色,能全部被磁铁吸引。
(猜想与假设)猜想一:剩余固体是Fe与Fe3O4:猜想二:剩余固体是_____。
(实验探究)
实验操作 | 实验现象及结论 |
_____ | _____ |
(实验结论)铁和水蒸气反应的化学方程式为_____。
(反思与交流)该黑色固体不可能是Fe2O3,理由是_____。
【题目】为了检测某石块样品中碳酸钙的含量,甲、乙、丙、丁四位同学用质量分数相同的盐酸与石块样品充分反应来进行实验测定(样品中的杂质不溶于水,且不与盐酸反应),测得数据如表:
甲同学 | 乙同学 | 丙同学 | 丁同学 | |
所取石块样品质量(g) | 10.0 | 10.0 | 10.0 | 10.0 |
加入盐酸的质量(g) | 10.0 | 20.0 | 30.0 | 40.0 |
烧杯中剩余物质的总质量(g) | 19.0 | 28.0 | 37.8 | 47.8 |
(1)碳酸钙中钙元素的质量分数为__________。
(2)10g石块样品完全反应,产生气体的质量为_________。
(3)求样品中碳酸钙的质量分数______(写出计算过程)。
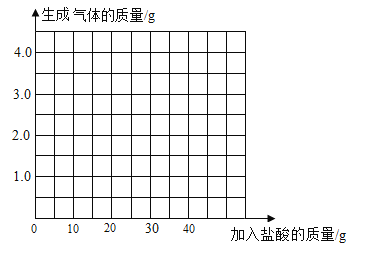
(4)请在图中画出加入稀盐酸的质量与生成气体的质量的变化关系。_____。