题目内容
某粗盐样品中含有可溶性的氯化镁、氯化钙杂质和不溶性的泥沙.常温下,将140g该粗盐样品溶解于水中,过滤得到不足3g泥沙和1000g溶液.取出500g溶液进行测定,其中含有镁元素1.2g,钙元素2g,氯元素42.6g.则原粗盐中氯化钠的质量分数约为( )A.83.6%
B.86.3%
C.88.1%
D.91.6%
【答案】分析:利用化合物的质量=元素质量÷化合物中该元素的质量分数,由镁元素、钙元素的质量计算出氯化镁和氯化钙的质量;再利用氯化镁、氯化钙两化合物的质量计算其中氯元素的质量;
然后利用测定出氯元素的总质量减去氯化镁、氯化钙中氯元素质量可求得氯化钠中氯元素质量,再利用元素质量与化合物质量的关系式,计算出氯化钠的质量;
最后,利用所计算氯化钠质量的2倍与140g粗盐的比,求得粗盐中氯化钠的质量分数.
解答:解:500g溶液中含氯化镁的质量=1.2g÷ ×100%=4.75g,则氯化镁中氯元素的质量=4.75g-1.2g=3.55g
×100%=4.75g,则氯化镁中氯元素的质量=4.75g-1.2g=3.55g
500g溶液中含氯化钙的质量=2g÷ ×100%=5.55g,则氯化钙中氯元素的质量=5.55g-2g=3.55g
×100%=5.55g,则氯化钙中氯元素的质量=5.55g-2g=3.55g
500g溶液中氯化钠所含氯元素的质量=42.6g-3.55g-3.55g=35.5g,则溶液中氯化钠的质量=35.5g÷ ×100%=58.5g
×100%=58.5g
则1000g溶液中氯化钠的质量=58.5g×2=117g
所以,原粗盐中氯化钠的质量分数=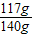 ×100%≈83.6%
×100%≈83.6%
故选A.
点评:在解答本题时,由于泥沙质量不能准确确定,因此,不能根据粗盐质量减去泥沙、氯化钙、氯化镁的方法求得氯化钠的质量.
然后利用测定出氯元素的总质量减去氯化镁、氯化钙中氯元素质量可求得氯化钠中氯元素质量,再利用元素质量与化合物质量的关系式,计算出氯化钠的质量;
最后,利用所计算氯化钠质量的2倍与140g粗盐的比,求得粗盐中氯化钠的质量分数.
解答:解:500g溶液中含氯化镁的质量=1.2g÷
 ×100%=4.75g,则氯化镁中氯元素的质量=4.75g-1.2g=3.55g
×100%=4.75g,则氯化镁中氯元素的质量=4.75g-1.2g=3.55g500g溶液中含氯化钙的质量=2g÷
 ×100%=5.55g,则氯化钙中氯元素的质量=5.55g-2g=3.55g
×100%=5.55g,则氯化钙中氯元素的质量=5.55g-2g=3.55g500g溶液中氯化钠所含氯元素的质量=42.6g-3.55g-3.55g=35.5g,则溶液中氯化钠的质量=35.5g÷
 ×100%=58.5g
×100%=58.5g则1000g溶液中氯化钠的质量=58.5g×2=117g
所以,原粗盐中氯化钠的质量分数=
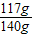 ×100%≈83.6%
×100%≈83.6%故选A.
点评:在解答本题时,由于泥沙质量不能准确确定,因此,不能根据粗盐质量减去泥沙、氯化钙、氯化镁的方法求得氯化钠的质量.

练习册系列答案
相关题目

